-

-
한국엘러간(대표이사 김은영)은 방광기능장애에 대한 보톡스주 치료의 보험급여가 10월 1일부터 적용된다고 밝혔다. 이번 급여 신설로 과민성방광 치료에 우선적으로 시행되는 행동치료를 포함한 적절한 보존요법과 항콜린제 치료에 실패한 신경인성 배뇨근 과활동성, 과민성 방광환자들은 보톡스주 치료옵션을 선택할 수 있게 됐다.이로써 기존에 1차 치료로 만족할 만한 효과가 없었던 환자들이 신경조정술이나 수술치료법 등 침습적 시술로 넘어가기 전 보톡스주를 통한 치료를 고려해볼 수 있게 될 전망이다. 방광기능장애에 가장 많이 사용되는 경구 약물치료의
제약단신
박상준 기자
2015.10.05 13:46
-

-

-

-
미국식품의약국(FDA)이 SGLT-2 억제제의 케톤산증 위험도를 강조하고 나섰다. 이는 2013년 3월~2014년 6월 6일 FDA 유해사건보고시스템(Adverse Event Reporting System)의 자료를 근거로 한 것으로, FDA는 "SGLT-2 억제제 치료와 연관된 당뇨병성 케토산증, 케토산증, 케토증이 20여건 보고됐다"며 이에 대한 경고문을 발표했다. 이번 경고문은 카나글리플로진, 다파글리플로진, 엠파글리플로진 SGLT-2 억제제 단독제제와 함께 카나글리플로진 + 메트포르민, 다파글리플로진 + 메트포르민 서방정
제약단신
임세형 기자
2015.05.19 06:18
-

-

INS·2세대 항히스타민제 효과 인정 일반적으로 알레르기 비염은 △ 알레르겐 회피 또는 환경관리 △ 약물치료 △ 면역치료(피하 주사제 혹은 설하정제) 등으로 치료한다. 이번 진료지침은 여러 약물요법 가운데서도 INS와 함께 부작용을 줄인 2세대 항히스타민제에 손을 들어주었다.세티리진, 레보세티리진, 로라타딘, 데스로라타딘, 펙소페나딘 등 2세대 항히스타민제를 비롯해 베클로메타손, 부데소니드, 시클레소니드, 플루니소리드, 플루티카손, 모메타손, 트리암시놀론 등의 비강내 코르티코스테로이드(INS) 등이 대표적 약물이다.우선 다학제 패널
호흡기/알레르기/감염
원종혁 기자
2015.02.24 07:01
-

-
미국식품의약국(FDA)이 아스트라제네카의 프로톤펌프억제제(PPI)인 에소메프라졸 서방형의 첫 번째 제네릭 제제를 승인했다. 에소메프라졸 제네릭은 테바(Teva) 제약의 자회사인 아이백스(Ivax) 제약이 생산하게 되며 20mg, 40mg 용량으로 출시된다. 적응증은 성인과 1세 이상 소아의 위식도역류질환(GERD) 치료, 비스테로이드성항염증제(NSAID)로 인한 위장관 궤양 위험도 감소, 헬리코박터 파일로리 감염 치료, 졸린거-엘리슨증후군 증 산과다분비 증상 치료 등이다. 중증 유해반응으로는 중증 설사를 비롯한 위 관련 문제가 꼽혔
제약단신
임세형 기자
2015.01.30 17:40
-
금연에 대한 국민 관심이 증가함에 따라 전자담배처럼 전자장치(공산품)에 충전해 사용하는 '액상향료'는 앞으로 의약외품으로 관리될 전망이다.식품의약품안전처(처장 정승)가 1월 26일자로 이 같은 내용의 '의약외품 범위지정' 일부 개정안을 행정예고 했다. 개정 내용이 시행되는 2016년 1월부터 전자장치를 이용해 사용(흡입)할 수 있는 니코틴 미함유 '액상향료'는 의약외품으로 허가·심사를 받아야 제조·수입할 수 있다.이번 행정예고는 액상향료를 금연용품으로 광고·판매하는 제품이 늘어나고 있는 상황에서 관리 강화 및 위해성 등의
보건복지
김지섭 기자
2015.01.26 12:47
-

-

-
-

-
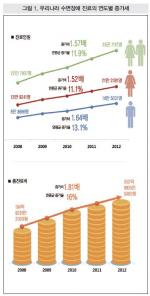
아주대학교병원 수면검사실이 개소 3년 10개월만에 검사 3천 건을 돌파했다.수면검사실은 수면 무호흡, 기면증, 수면중 이상 행동, 불면증 등 여러 종류의 수면 질환을 진단하고 치료하기 위하여 정식 수면다원검사와 이동형 수면검사은 물론이고, 기면증 진단을 위한 다중수면 잠복기 검사 등을 시행하는 곳이다.수면검사실에서는 수면다원 검사 2353건(78%), 양압기 적정 압력 검사 339건(11%), 수면 분할 검사(split-night study) 299건(10%), 다중 수면 잠복기 검사(MSLT) 43건(1%) 등으로 10월 22일
병원·개원가
박선재 기자
2014.10.27 10:45
-

-
미국식품의약국(FDA)이 금연약물인 바레니클린의 신경정신건강학적 유해사건에 대한 블랙박스 경고문을 재차 강조하고 나섰다. FDA는 최근 바레니클린 제조사인 화이자가 제출한 승인 후 임상시험(post-marketing study) 검토 결과 "이 연구가 바레니클린의 전반적인 신경정신건강학적 유해사건 모두를 확인한 것은 아니다"며 기존의 블랙박스 경고문을 유지하겠다고 밝혔다. 바레니클린은 2006년 승인받은 이후 자살충동, 불안정한 행동, 졸림 등 중증 부작용 문제가 지속적으로 지적돼 왔고, 2009년 이에 대한 블랙박스 경고문이
제약단신
임세형 기자
2014.10.15 16:36
-

-
