2021년 급여적정성 재평가 대상 확정…엔테론 등 157품목
주요제품 6품목의 지난해 3분기 기준 매출 규모 970억원

[메디칼업저버 정윤식 기자] 콜린알포세레이트 제제의 뒤를 이을 급여적정성 재평가 대상 성분이 확정된 가운데, 이들의 대표 제품 6종만으로도 1000억원가량의 시장이 형성된 것으로 나타났다.
보건복지부는 최근 건강보험정책심의위원회를 통해 2021년 상반기에 실시할 급여적정성 재평가 대상 성분 5개를 선정·발표했다.
선정된 성분은 △비티스비니페라(Vitis vinifera) △아보카도-소야(avocado-soya unsaponifiables) △은행엽엑스(Ginkgo biloba leaf ext.) △빌베리건조엑스(Bilberry fruit dried ext.) △실리마린(Silymarin, milk thistle fruit ext.) 등이다.
이번 5개 성분에 대한 재평가는 시범평가였던 콜린알포세레이트 제제와 달리 본평가에 해당한다.
2006년 선별등재제도 도입 이전에 등재된 의약품이며, 5개 성분 안에는 제약사 98곳의 157품목이 포함된 것으로 알려졌다.
이번 재평가 성분들은 콜린알포세레이트와 마찬가지로 주요 외국 A8(미국, 영국, 프랑스, 이탈리아, 일본, 독일, 스위스, 캐나다)에서 건강기능식품으로 분류되는 의약품이라는 게 특징이다.
결국 정부는 지난해 시범평가격인 콜린알포세레이트에 이어 지속적으로 의약품의 재평가를 추진하겠다는 원칙을 재확인한 셈인데, 자연스럽게 이들 성분 제품의 시장 규모에 이목이 쏠리고 있다.
현재 비티스비니페라는 한림제약의 엔테론과 아주약품의 안탁스, 아보카도-소야는 종근당의 이모튼, 은행엽엑스는 유유제약의 타나민, 빌베리건조엑스는 국제약품의 타겐에프, 실리마린은 부광약품의 레가론 등이 대표제품으로 꼽힌다.
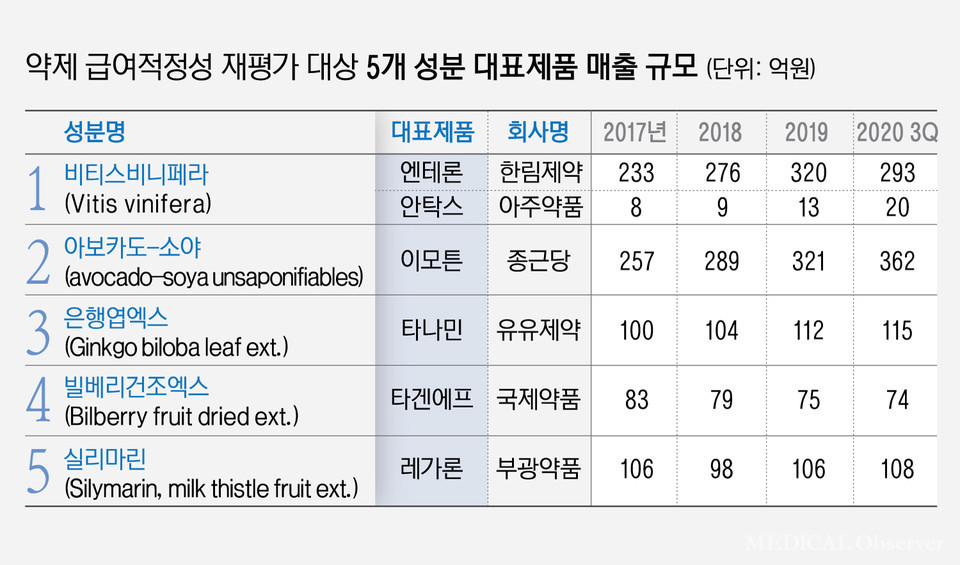
시장조사기관 아이큐비아 자료를 토대로 대표제품만 별도로 집계한 결과, 혈액순환과 유방암치료로 인한 림프부종 보조요법, 망막·맥락막 순환 등에 효능·효과가 있는 비티스비니페라 성분의 엔테론과 안탁스는 2020년 3분기에 각각 293억원, 20억원의 매출을 올렸다.
엔테론은 2017년 233억원, 2018년 276억원, 2019년 320억원으로 매출 규모가 꾸준히 상승했으며 안탁스도 지속적인 상승 곡선을 그렸다(8억원→9억원→13억원).
골관절염과 치주질환에 효과를 보이는 아보카도-소야의 주요제품인 이모튼은 2017년 257억원 이후 매년 새로운 기록을 갱신해 2020년 3분기 기준 362억원까지 매출 규모가 상승했다.
은행엽엑스는 유유제약의 타나민이 대표제품이며 뇌혈액순환과 동맥경화성 혈관증에 효능을 나타낸다.
타나민은 2017년 100억원, 2018년 104억원, 2019년 112억원, 2020년 3분기 115억원까지 매출이 올랐다.
반면, 빌베리건조엑스 성분의 타겐에프는 시장 규모가 점차 줄어들고 있다.
2017년 83억원의 매출이 79억원(2018년)→75억원(2019년)→74억원(2020년 3분기)으로 서서히 주저앉은 것.
간염과 간경변에 효능·효과가 있는 것으로 알려진 부광약품의 레가론은 엔테론, 안탁스, 이모튼처럼 꾸준히 상승하지 않고 매년 증감을 반복하는 중이다.
레가론의 매출액은 2017년 106억원, 2018년 98억원, 2019년 106억원, 2020년 3분기 108억원이다.
즉, 5개 성분의 주요 제품 6종만으로도 2020년 3분기 기준 매출액이 972억원을 기록한 것으로 집계된 것이다.
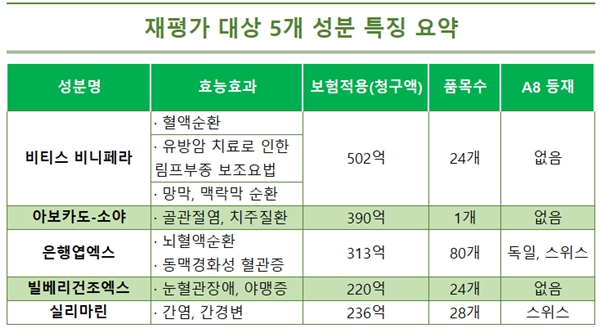
참고로 재평가 대상 비티스비니페라, 아보카도-소야, 은행엽엑스, 빌베리건조엑스, 실리마린에 포함되는 의약품의 수는 각각 △24개 △1개 △80개 △24개 △28개로, 복지부가 추산한 이들의 보험적용 청구액은 각각 △502억원 △390억원 △313억원 △220억원 △236억원 총 1661억원이다.
A8의 등재의 경우 은행엽엑스와 실시마린만 독일 및 스위스에서 의약품의 분류됐다.
한편, 복지부는 2월 중에 재평가 계획을 공고하고 해당 제약사에 그 내용을 통보할 계획이다.
이후 건강보험심사평가원과 함께 재평가 대상 약제에 대해 임상적 유용성 문헌 검토 등을 통해 급여 적정성을 재평가한 뒤 이르면 가을에 그 결과를 건정심에 보고할 방침이다.
관련기사
- 政, 약제 재평가 집행정지 손실 보전 위한 제도개선 마련
- 사라진 '콜린' 간판…자진취하+행정처분 110품목 이상
- [송년특집] 임상재평가 시범사업 첫 타자 '콜린알포세레이트'
- "참여 할래? 말래?"…두 그룹으로 나뉜 콜린알포 임상재평가
- 약제 급여적정성 1차 본평가 대상 내달 중 공개
- 콜린알포, 요양급여 대상변경인가 기준변경인가
- 콜린알포 소송 첫 만남에 '유용성' 시비는 없었다
- 막 오른 5개 성분 급여 재평가...19일까지 자료 제출해야
- 비급여 관리 힘싣는 심평원, 올해 표준화된 비급여 파일 생성 목표
- SK케미칼, '기넥신에프정 240mg' 출시
- 한림제약, '엔테론' 재평가 계획 제출…올해 첫 사례
- 식약처, 의약품 재평가 기한 연장 기준 마련
- 종근당 '이모튼캡슐' 효능·효과 범위 축소
- 재평가 성분 중 3개 급여 불인정, 엔테론만 일부 유지
- 콜린알포 임상재평가 환수협상 완료, 44개 제약사와 체결


단순한 건강식품정도 네요! 많은 회사에서 생산하고
판매 하는걸보니 리베이트 운영약물 아닌지 처방하는 의사들도 조금의심스럽네요