선두 암젠 소토라십 이은 후발주자 도전
미라티·릴리, 각각 1상, 전임상서 긍정적 결과
[메디칼업저버 양영구 기자] 글로벌 제약업계가 KRAS G12C 유전자 돌연변이를 표적하는 항암제 개발에 뛰어들고 있다.
KRAS는 세포 성장과 증식이 가장 빈번하게 돌연변이되는 종양 유전자를 촉진하는 핵심 매개체다.
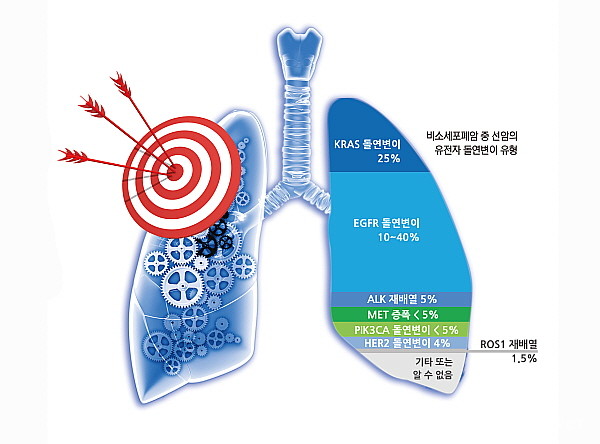
특히 KRAS G12C 유전자 돌연변이는 비소세포폐암(NSCLC)의 약 14%, 결장직장암의 4%, 췌장암의 2%에서 나타나는 것으로 알려진다.
하지만 현재 미국식품의약국(FDA)으로부터 정식으로 허가받은 KRAS G12C 유전자 돌연변이를 표적하는 항암제는 없는 실정이다.
현재 암젠이 전 세계적으로 가장 앞서는 상황이다.
암젠 소토라십은 올해 1월 열린 국제폐암컨퍼런스(WCLC 2020)에서 CodeBreak100 임상2상 결과를 공개한 바 있다.
이런 가운데 후발 주자들도 개발에 적극 나선 상태다.
미라티 '아다그라십'...KRYSTAL-1 연구서 효과 입증
미라티테라퓨틱스의 KRAS G12C 억제제 아다그라십(프로젝트명 MRTX849)은 소토라십의 뒤를 바짝 추격하고 있다.
최근 열린 제32차 EORTC-NCI-AACR 심포지엄에서 미국 하버드의대 Pasi A. Janne 교수 연구팀은 아다그라십의 임상1/1b상 연구 KRYSTAL-1 결과를 발표했다.
이 연구는 이전에 화학요법을 받은 KRAS G12C 유전자 돌연변이를 갖고 있는 비소세포폐암 환자 110명을 대상으로 아다그라십의 안전성, 약동학(PK), 효능 등을 평가한 임상시험이다.
연구에서는 110명의 환자에게 아다그라십 600mg으 1일 2회 단독요법으로 경구투여했고, 그 중 2020년 8월 30일까지 치료를 진행한 79명의 데이터가 포함됐다.
연구 결과, 아다그라십군의 객관적반응률(ORR)은 45%로 나타났다.
또 평가 가능한 환자 51명의 질병통제율(DCR)은 96%였는데, DCR은 평균 3.6개월 이어졌다.
특히 가장 오랜 기간 동안 추적된 환자 14명(중앙값 9.6개월)의 ORR은 43%로 나타났다. 이 중 4명은 11개월 이상 치료가 지속됐다.
일반적으로 보고된 치료관련 부작용(TEAE)은 메스꺼움(54%), 설사(48%), 구토(34%), 피고(28%), ALT 증가(23%) 등의 순으로 나타났고, 3~4등급 치료관련 이상반응은 저나트륨혈증(3%)이었다.
연구팀은 "아다그라십은 KRAS G12C 유전자 돌연변이 환자에게 광범위한 질병통제율과 지속적인 반응이 관찰됐다"며 "아다그라십은 KRAS G12C 억제제의 역할에 최적화돼 있다"고 강조했다.
릴리, 임상1상 중단 부침 딛고 재도전
일라이릴리도 KRAS G12C 유전자 돌연변이 표적 항암제 개발에 재도전한다.
릴리는 초기 차세대 항암제 포트폴리오 3가지 중 하나로 꼽았던 KRAS G12C 억제제 LY3499446의 개발을 중단한다고 지난해 발표한 바 있다.
2019년 12월 KRAS G12C 유전자 돌연변이를 가진 비소세포폐암, 대장암 등 진행성 고형암 환자 230명을 대상으로 LY3499446 단일 및 병용투여의 안전성과 내약성, 효능 등을 평가하는 임상1상을 중단한 것이다.
임상에서 발견된 약물 독성이 이유다.
하지만 최근 릴리는 KRAS G12C 저해제 개발에 다시 뛰어들었다.
오는 4월 10일 열리는 미국암연구학회(AACR 2021) 초록에 따르면, 릴리는 새로운 KRAS G12C 저해제 LY3537982 임상1상을 올해 진행할 방침이다.
릴리가 공개한 LY3537982의 전임상 결과에 따르면 이 후보물질은 암젠 소토라십, 미라티 아다그라십과 비교해 더 높은 선택성과 효능을 보인다.
전임상 결과, LY3537982의 Kinact/Ki 값은 248,016 M-1 s-1로 암젠 소토라십(7,220 M-1 s-1), 미라티 아다그라십(35,000 M-1 s-1)에 비해 높았다.
특히 KRAS-G12C 돌연변이 H358 폐암 세포주에서 IC 50값이 3.35nM으로 KRAS-GTP 로딩을 억제했다. 반면, 소토라십과 아다그라십은 각각 47.9 nM 및 89.9 nM의 IC 50 값을 보였다.
또 LY3537982는 IC 50 값이 0.65nM인 H358 세포에서 phospho-ERK를 억제했지만, 소토라십과 아다그라십은 IC 50 값이 각각 13.5 nM, 14 nM으로 나타났다.
아울러 KRAS G12C 유전자 돌연변이를 보유한 다중 이종 이식 또는 환자 유래 이종 이식 모델에서 3~30mg/kg 1일 1회 투약(QD) 또는 1일 2회 투약(BID)에서 유의한 종양 성장 억제 등 다양한 종양 활성을 나타냈다.
병용투여 전략도 내세운다.
메커니즘 기반 약물조합 스크린에서 LY3537982는 버제니오(성분명 아베마시클립), AurA 억제제 LY3295668, 얼비툭스(세툭시맙) 등 체외 및 체내 종양 예방 활동을 높일 수 있는 특정 표적항암제와의 시너지 효과를 발휘할 수 있다는 것을 확인했기 때문이다.
릴리는 "이 같은 LY3537982의 데이터는 더 광범위하고 내구성이 높은 종양 예방 활동을 달성할 수 있을 것"이라고 강조했다.
관련기사
- 아미반타맙·소토라십 등 5종 희귀의약품 신규 지정
- 암젠 소토라십, 임상2상에서도 '성공' 가능성 ↑
- 암젠, 폐암 신약 '소토라십' FDA 허가 신청
- 암젠 소토라십, 임상 1상임에도 승리라 불리는 이유는?
- KRAS 유전자 변이 폐암 신약, 세상에 나온다
- [ESMO 2021] 아다그라십, 결장직장암도 가능성↑
- 암젠 KRAS G12C 표적 치료제 '루마크라스' 식약처 허가
- 암젠 루마크라스, KRAS 변이 폐암서 확고한 입지 다져
- 글로벌 제약, 뇌전이 비소세포폐암 정복 나서
- 난공불락 '췌장암' 철옹성 무너지나
- KRAS 억제제 대장암 분야 도전 '성공적'
- 루마크라스 VS 크라자티, KRAS 표적항암제 경쟁 시작
- 미라티 폐암 신약 시트라바티닙, 임상3상 실패

