심평원, 제10차 약평위 심의 결과 발표
6개 약제 결정신청·1개 약제 급여확대 평가
타그리소, 폐암 1차 치료제로 급여 확대

[메디칼업저버 박서영 기자]한국아스트라제네카(AZ)의 타그리소가 비소세포폐암 1차 치료제로 급여가 확대되면서 환자 치료의 폭이 넓어질지 눈길을 끈다.
건강보험심사평가원은 지난 8일 2023년 제10차 약제급여평가위원회에서 심의한 결과를 발표했다.
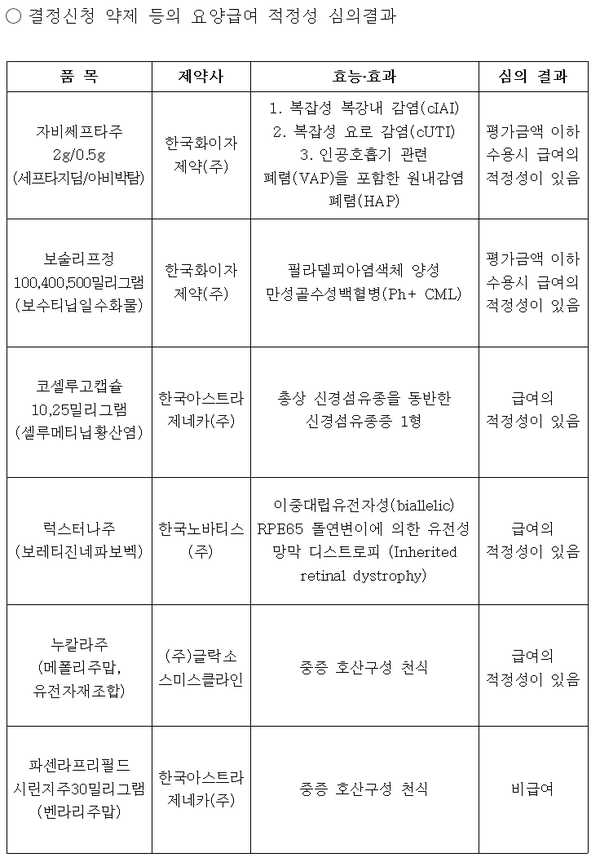
이번 약평위에서는 총 6개의 약제에 대한 평가가 이뤄졌다. 이 가운데 급여확대 신청 약제인 AZ의 타그리소(오시머티닙)는 폐암 1차 치료제로 급여 적정성을 인정받았다.
타그리소는 2016년 국내 허가 취득 후 폐암 2차 치료제로 사용돼왔다. 그러나 1차 치료로 사용 시 임상적 유용성 면에서 효과를 부정할 수 없다는 전문가들의 의견이 있었고, 이에 지난 3월에는 심평원 암질환심의위원회에서 1차 치료제 대한 급여 기준이 설정되기도 했다.
타그리소 급여가 확대되면서 앞으로 환자가 치료 옵션을 선택하는 데 있어 범위가 넓어질 것으로 전망된다.
이외에도 AZ의 코셀루소캡슐(셀루메티닙황산염) 10mg, 25mg가 총상 신경섬유종을 동반한 신경섬유종증 1형에 대한 급여 적정성을 인정받았다.
또 한국노비타스의 럭스터나주(보레티진네파보벡)과 글락소미스클라인의 노칼라주(메폴리주맙) 역시 각각 이중대립유전자성(biallelic) RPE65 돌연변이에 의한 유전성 망막 디스트로피와 중증 호산구성 천식에 급여 적정성을 인정받았다.
한국화이자의 자비쎄프타주 2g/0.5g(세프타지딤/아비박탐)과 보술리프정(보수티닙일수화물) 100mg, 400mg, 500mg은 조건부 급여 인정을 받았다.
이번 약평위를 통과한 약제들은 이후 국민건강보험공단과의 약가 협상과 건강보험정책심의위원회(건정심) 의결을 거쳐 보험급여가 최종적으로 이뤄진다.
심평원은 "약제의 급여기준은 식품의약품안전처 허가사항의 효능효과 범위 내에서 임상문헌, 국내 및 외국 가이드라인, 전문가 의견에 따라 다르게 설정될 수 있으며, 후속절차 진행과정에서 급여여부 및 급여기준이 변경될 수 있다"고 설명했다.
관련기사
- 레바피미드·레보설피리드, 건강보험 급여 유지
- “약평위 참여 위원에 공단 포함돼야…지속적으로 설명할 것”
- 레테브모, '국내 유일' RET 표적치료제 굳히기 돌입하나
- 공단 제외된 제9기 약평위…건보노조, 심평원 역할 조정 요구
- 레블로질, 약평위 문턱 못 넘어…젬퍼리는 급여 적정성 인정
- [WCLC 2023] 타그리소, 항암화학 병용으로 EGFR 변이 폐암 1차치료 입지 강화
- [WCLC 2023]"FLAURA2, EGFR 변이 폐암 완치 향한 연구 기반될 것"
- 심평원, 제9기 약평위 위원 76명 위촉
- 타그리소 내성 EGFR 폐암 리브리반트·렉라자 효과 확인
- 아토피 피부염 치료제 아트랄자, 약평위 통과

