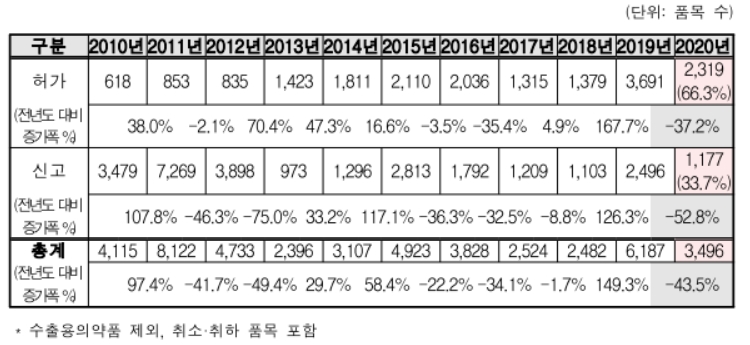
허가 2319건·신고 1177건 총 3496건…2019년 총 6187건에서 급락
희귀의약품 및 신약 품목 허가 증가…순환계용의약품 비중 가장 높아

[메디칼업저버 정윤식 기자] 지난해 화학의약품, 생물의약품 등 전체 의약품의 허가·신고 전체 품목 수가 전년에 비해 대폭 감소한 것으로 나타났다.
2020년 총 3496품목이 허가·신고 됐는데, 이는 2019년 6187품목 대비 약 43.5% 감소(2691품목)한 수치다. 특히, 제조품목 허가·신고 품목 수가 45%가량 급감했다(2712품목).
위탁(공동) 생동 시험 자료 제출에 따라 급증했던 2019년도 제네릭의약품 허가·신고 품목 수가 2020년에 다시 감소한 데 기인한 것으로 파악되는데, 실제로 그 전년도인 2018년 허가·신고(2482품목)보다는 1.4배 증가했다.
식품의약품안전처는 최근 의약품 연구·개발 지원 등을 위해 '2020년도 의약품 허가 보고서'를 발간했다.
전체 3496품목 중 허가 2319품목, 신고 1177품목
지방청 허가품목이 본부보다 약 2.2배 더 많아
허가·신고 총 3496품목 중 허가품목은 6.3%(2319품목), 신고품목은 3.7%(1117품목)로 집계됐다.
처리기관별로는 본부 처리품목이 21.1%(738품목)인 반면 지방청 허가·신고품목은 78.9%(2,758품목)였다.
국내 제조판매품목이 95.1%(3323품목)에 달한 것에 비해 수입품목은 4.9%(173품목)로 소수였고 완제의약품이 92.4%(3229품목), 원료의약품은 2.0%(69품목), 한약재 5.7%(198품목)로 분류됐다.
완제의약품과 한약재 품목 수는 감소한 반면 수입품목 및 원료의약품 품목 수는 전년도와 유사한 수준을 유지했다.
한약재를 제외하면 완제의약품(97.9%)이 원료의약품(2.1%)보다 월등히 많았고, 완제의약품 3229품목 중 전문의약품은 78.2%(2525품목), 일반의약품 21.8%(704품목)다.
허가품목만 살펴보면 전체 2315품목 중 지방청 허가가 1582품목(68.3%)으로 본부 허가 733품목(31.7%)보다 2.2배가량 많았다.
이는 지방청 허가 대상인 제네릭의약품 허가가 본부 허가 대상인 자료제출의약품보다 상대적으로 많다는 것을 의미하는데, 지방청 허가 의약품 중 98.7%인 1562품목이 제조품목이었다.
허가·신고품목의 제조품목 및 수입품목 현황을 분석한 결과, 허가품목이 더 높은 비중을 차지했다
제조품목의 경우 허가 65.9%(2190품목), 신고 34.1%(1133품목)였고 수입품목의 경우 허가 74.6%(129품목), 신고 25.4%(44품목)였다.
코로나19 치료제 신속 허가 특징
신약 및 희귀의약품 허가건수 증가
식약처는 지난해 7월 특례수입 승인을 통해 공급한 길리어드사이언스코리아의 코로나19(COVID-19) 치료제 '베클루리주정맥주사용동결건조분말(렘데시비르)'를 국내 환자의 안정적 치료를 위해 수입의약품으로 신속 허가했다.
이는 국민 보건 위기에 선제적으로 대응해 치료제 의약품 공급 체계를 구축한 사례로 2020년 의약품 허가·신고 현황의 주요 특징이다.
희귀의약품 품목허가 건수는 2016년 34품목에서 2019년 11품목으로 다소 감소하는 추세를 보였으나, 지난해 상승세로 돌아서 24품목(14개 성분)이 허가됐다.
2015년 7월 '의약품 등의 안전에 관한 규칙' 개정 규정에 따라 강화된 희귀의약품의 품목허가 제출자료 요건을 업계가 충분히 소화하고 희귀의약품에 대한 안전관리 수준도 높아졌기 때문으로 판단된다.
당시 개정 규정에는 △GMP 실시상황 평가자료 △기준 및 시험방법 자료 △위해성 관리 계획 제출 필요 등이 포함됐다.
신약은 2018년 15품목(12성분)에서 2019년 35품목(21성분), 2020년 40품목(20성분)으로 꾸준히 늘고 있으며 그 중 수입 신약 35개, 국내 제조 신약 5개가 허가됐다.
제품 특성별로는 화학의약품 34품목, 생물의약품 6품목이 허가됐고 약효군별로는 항암제 13품목이 허가돼 전체 32.5%로 높은 비중을 차지했다.
국내 개발 개량신약 허가는 6개로, 전년 대비 감소했지만 바이오시밀러가 2품목 허가돼 전년과 유사한 전체 허가 건수 수준을 유지했다.
화학의약품 국내신약 5개 품목은 슬관절염 치료제 1개와 항전간제 4개이며, 생물의약품 수입신약 6개 품목은 발작성 야간 혈색소뇨증(PNH)치료제와 황반변성치료제 등이다.
'새로운 조성 제품' 허가 증가…순환계의약품 비중 높아
지난해 허가된 안전성·유효성 심사 자료제출 대상인 자료제출의약품 326품목 중 '새로운 조성 제품'이 182개(55.8%)를 차지해 집중적으로 개발된 양상을 보였다.
특히 고지혈증 치료제의 유효성분인 '로수바스타틴칼슘'을 함유한 고혈압·고지혈증 복합제로 개발이 높은 비중을 차지했다(154품목, 84.6%).
특허 회피 목적으로 활용되는 '새로운 염 또는 이성체'를 유효성분으로 하는 의약품 개발도 2019년 2품목에서 2020년 74품목으로 크게 증가했는데, 이는 당뇨병 치료제에 쓰이는 유효성분의 새로운 염 개발에 따른 것으로 업계에서 당뇨병 시장 선점을 위한 각각의 생존 전략에 따른 영향이다.
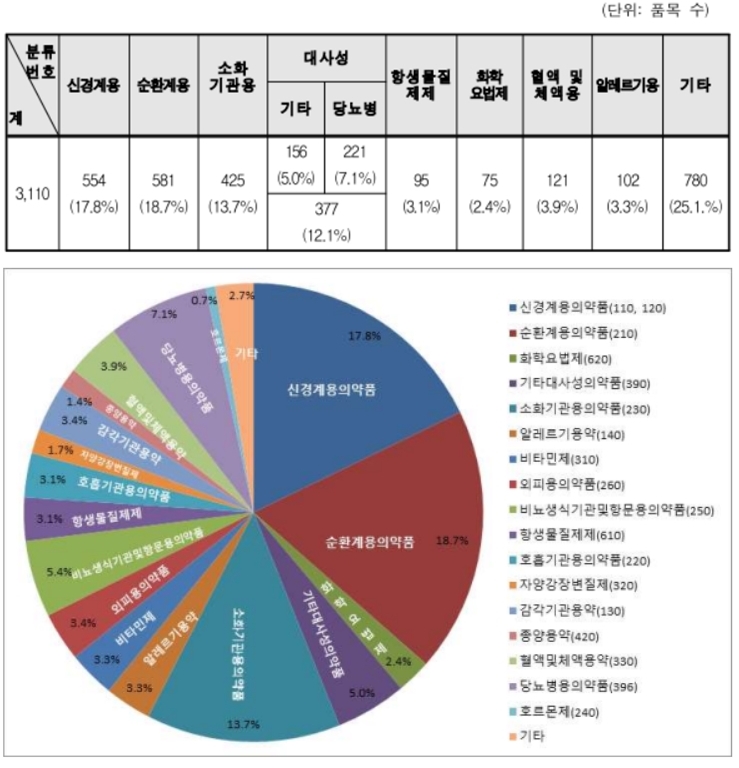
약효군별 전체 3110개 허가 품목 중 '혈압강하제' 등이 포함된 '순환계용의약품'이 581품목으로 가장 많이 허가됐다(18.7%).
이는 2019년 902품목을 허가해 전체 18.8%를 차지했던 것과 비슷한 수준이며 고령화 등 혈압약 시장의 지속적인 팽창에 따른 것으로 보인다.
이어 △해열·진통·소염제 등 신경계용의약품 554품목(17.8%) △소화기관용의약품 425품목(13.7%) △기타의 대사성의약품 및 당뇨병용제 337품목(12.1%) △혈액 및 체액용약 121품목(3.9%) △알레르기용약 102품목(3.3%) △항생물질제제 95품목(3.1%) 등의 순으로 허가됐다.
생물학적제제, 국내 제조 18품목·수입 2품목 허가
지난해 허가된 생물학적제제는 20품목(제조 18, 수입 2)이며 백신 9품목, 보툴리눔 독소 7품목, 혈액제제 4품목으로 나뉜다.
2017년 이후 생물학적제제의 품목허가는 감소 추세였으나 지난해 다시 반등을 그렸다.
허가된 백신은 제제별로 인플루엔자백신 4품목, 수두백신 1품목, A형간염백신 1품목, 폴리오백신 1품목, 폐렴백신 1품목, 혼합백신 1품목이다.
구체적으로 인플루엔자 백신은 보령바이오파마의 내수용 2품목(아플루리아쿼드프리필드시린지, 보령플루XI테트라백신프리필드시린지)과 SK바이오사이언스의 수출용 2품목(스카이셀플루4가프리필드시린지, 스카이셀플루프리필드시린지)이 해당된다.
수두백신은 GC녹십자의 '배리셀라'이며, A형간염백신은 보령바이오파마의 '보령A형간염 백신프리필드시린지'가 허가됐다.
폴리오백신으로는 LG화학의 '유폴리오', 폐렴백신으로는 SK바이오사이언스의 '스카이뉴모프리필드시린지'가 수출용으로 각각 품목 허가됐다.
혼합백신은 사노피파스퇴르의 '헥사심프리필드시린지'가 생후 2개월 이상의 영아에서 디프테리아, 파상풍, 백일해, B형 간염, 폴리오(소아마비) 예방 및 b형 헤모필루스 인플루엔자(Hib)에 의해 발생하는 침습성 질환 예방을 목적으로 허가 받았다.
한편 보툴리눔 제제는 2016년 4품목, 2017년 2품목, 2018년 1품목, 2019년 2품목(내수 1, 수출 1) 등 특별한 증가세가 없다 2020년에만 수출용으로 7품목이 신규로 허가돼 눈길을 끈다.

