이전 감염병에 일부 사용된 혈장치료, 코로나19에는 근거 부족
FDA, 혈장치료 작년 8월 긴급 승인...지난달 개정으로 사용 제한
최근 RCT 결과, 경증 코로나19 입원환자에만 일부 이점
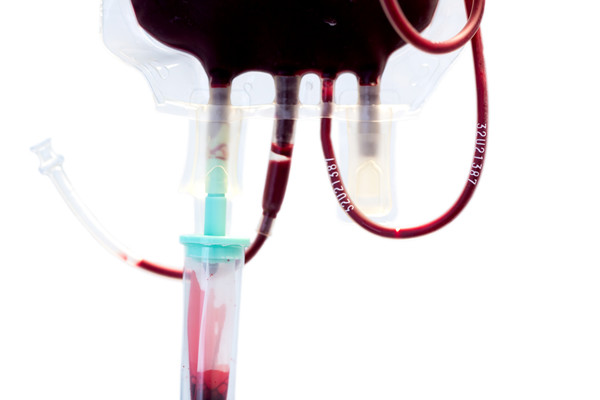
[메디칼업저버 주윤지 기자] 미국 보건당국이 코로나19(COVID-19) 환자에 혈장치료 사용을 이전보다 특정 인구로 제한했다.
미국식품의약국(FDA)은 지난달 5일 혈장치료에 대한 허가 사항을 최신 근거에 따라 수정했다면서 이번 개정으로 ▲항체 적정농도가 높은 고역가(high-titer) 혈장치료 사용만 허용했다.
FDA는 고역가 혈장치료를 ▲초기 감염 단계에 해당되는 코로나19 입원환자 또는 ▲적절한 항체반응을 생성하지 못하는 체액성면역이 손상된 환자에게만 허용했다.
'혈장치료(convalescent plasma)'란 질병에서 회복(완치)된 사람의 혈액에서 항체가 있는 혈장을 분리해 환자에게 수혈하듯 투입하는 치료법이다.
회복기 혈장치료는 공장 등에서 생산되는 '항체치료(antibodies therapy)'와 달리 회복한 환자가 기증한 혈장을 사용하며, 이는 중동호흡기증후군(MERS), 중증급성호흡증후군(SARS), 에볼라바이러스 등 감염병 치료에 사용됐다.
이번 개정안은 지난해 FDA가 코로나19에 혈장치료를 긴급사용승인(EUA) 절차로 허가한 것보다 사용 폭을 좁힌 것이다.
FDA는 지난 8월 23일 코로나19 치료제가 부족하고 혈장치료가 제공하는 이점이 위험을 능가한다고 판단해 혈장치료를 특정 제한 없이 긴급승인했다.
다만 당시 미국 의료단체들은 근거 미확립 문제로 FDA와 같은 입장을 취하지 않았다.
미국국립보건원(NIH) 지침 패널은 검토 가능한 근거 기반으로 혈장치료를 권고하거나 비권고할 수 없다고 선을 그었다.
또한 NIH는 지난 2일(현지시간) 최근 혈장치료가 입원하지 않은 경증 코로나19 환자군에 효과가 없었다면서 관련 연구를 중단했다고 밝혀 혈장치료에 대한 입장을 보다 예의주시하는 것으로 평가된다.
미국전염병학회(IDSA) 및 미국혈액은행협회(AABB)는 혈장치료를 제한적으로만 권고했다.
IDSA·AABB는 혈장치료를 코로나19 임상시험에서만 사용하도록 제한했고, 중증·중환자실 환자는 혈장치료로 혜택받을 가능성이 작어 혈장치료를 사용하면 감염 초기에만 사용하는 것을 권고했다.

국내에서 혈장치료는 선정된 몇몇 의료기관에서만 중증 코로나19 입원환자에 수혈하는 등 사용할 수 있는 것으로 조사됐다.
질병관리청 혈액안전감시과 관계자에 따르면 보건복지부는 혈장치료 관련 환자 가이드라인을 제공했고, 이는 법적 효력이 있는 지침보다 의료기관에서 전반적으로 적용할 수 있는 안내서(guidance) 수준에 머문다.
이외 국립보건연구원, 국립감염병연구소, 녹십자는 혈장치료체 'GC5131A'를 공동 개발해 현재 최소 60명을 포함한 2상 임상시험을 진행 중이다. GC5131A는 코로나19 완치자의 혈장에서 면역원성을 갖춘 항체를 추출해 만든 의약품이다.
코로나19에 혈장치료 주목받았지만 근거는 여전히 부족
이처럼 코로나19 혈장치료 및 혈장치료제가 국내외 주목되고 있지만, 의료계는 관련 근거가 부족하다고 여러 차례 경고했다.
세계보건기구(WHO)는 특히 FDA가 코로나19 혈장치료를 긴급승인하자 "관련 근거 수준이 매우 낮다"면서 혈장치료는 실험적인 요법으로 제한하고 추가적인 연구가 필요하다고 피력했다.
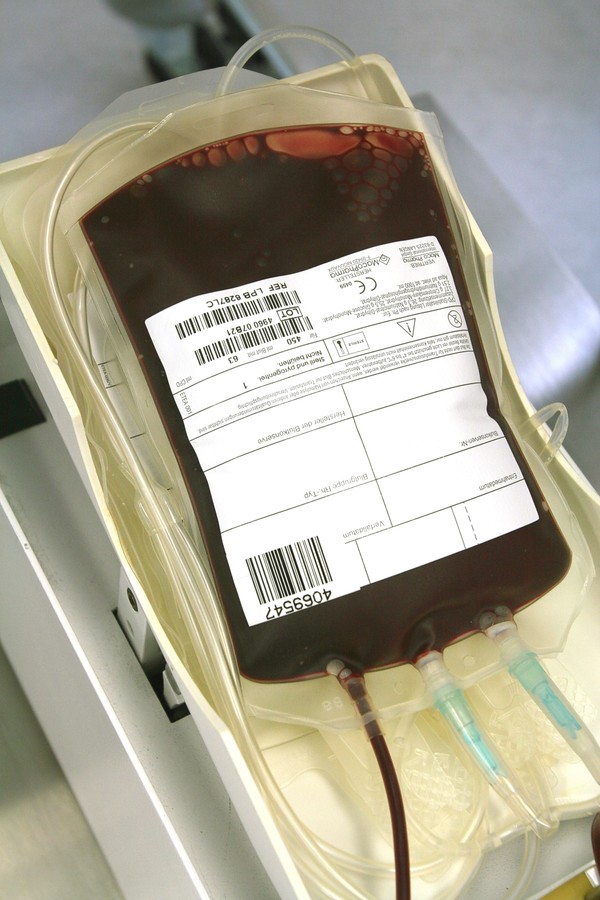
미국 감염병 전문가인 미시시피 밸리 지역혈액센터(Mississippi Valley Regional Blood Center) Louis M. Katz 교수도 최근 논평을 통해 "코로나19 혈장치료를 초기에 검토한 대부분은 무작위 대조군 연구가 아닌 관찰연구였으며, 연구에서 사용된 혈장치료는 통일되지 않고 정확한 환자 분류도 부족해 통계적 검정력 부족(statistically underpowered)한 문제가 있었다"고 설명했다.
따라서 지금까지 회복기 혈장치료 사용을 격려하는 임상근거는 부족하고, 동시에 혈장치료를 비권고할만한 근거도 없는 것이다.
특히 현재 근거에 따르면 코로나19 혈장치료는 과다혈증, 수혈관련급성폐장애, 알레르기 등을 제외하고 예상치 못한 중증 안전성 문제가 보고되지 않았고 항체의존면역증강(antibody-dependent enhancement, ADE) 사례도 없었다.
이에 Katz 교수는 "코로나19 감염이 늘고, 코로나19 치료제가 부족하고, 혈장치료에 이어지는 논쟁을 고려하면 높은 수준의 다기관 무작위 대조군 연구가 필요(most welcome)하다"고 했다.
아울러 지난 18일 국제학술지 'New England Journal of Medicine'에 알헨티나에서 진행된 무작위 대조군 연구 2편이 동시에 실렸다.
먼저 PlasmAr 연구는 중증 코로나19 환자 333명을 포함했고, 이들은 2:1 비율로 혈장치료(n=228) 또는 위약(n=105)을 받도록 무작위 배정받았다.
연구 결과, 중증 코로나19 환자에 혈장치료는 위약과 유의미한 효과 차이가 없었다(OR 0.83, 95% CI 0.52~1.35, P=0.46).
전체 사망률은 혈장치료군에 10.96%, 위약군에 11.43%로 두 치료군 간 -0.46%p 차이가 있었지만, 이는 통계적으로 유의미하지 않았다(95% CI -7.8~6.8).
다만 중증 이상반응과 부작용은 두 치료군 간 유사했다.
이어 무작위 이중 눈가림 대조군 INFANT-COVID-19 연구에서는 높은 역가 혈장으로 조기치료를 받은 65세 이상 경증 입원환자는 위약으로 치료받은 환자군보다 코로나19 악화 위험이 더 낮았다.
결과에 따르면 조기 혈장치료는 코로나19 감염증 악화를 위약보다 유의미하게 48% 낮췄다(RR 0.52, 95% CI 0.29~0.94, P=0.03).
INFANT-COVID-19 연구는 65세 이상 경증 코로나19 환자 160명을 포함했지만, 연구 당시 지역 감염증이 상당히 감소해 연구는 조기 중단됐다.
Katz 교수는 "현재 혈장치료는 (INFANT-COVID-19) 연구에서 포함된 환자와 유사한 감염 기간, 중증도, 중증질환 진행 위험도 특징을 보이는 코로나19 환자에 제한해야 한다"면서 "고위험 젊은 환자 또는 면역결핍 환자도 이러한 특징이 있으면 혈장치료를 고려할 수 있다"고 제안했다.
이어 "중증질환 진행 가능성 있는 초기 감염 환자를 제외하고 코로나19 환자에 통제 없이 혈장치료를 동정적으로 사용(compassionate use)하는 것은 피해야 한다"면서 혈장치료 사용 혼란을 해소하는 취지로 설명했다.
관련기사
- 코로나19 치료제 렉키로나 연구자 임상 차원 투여 진행
- GC녹십자, 코로나19 혈장치료제 3차 추가 생산 완료
- WHO 비권고한 렘데시브르...미국전염병학회는 권고 왜?
- GC녹십자, 코로나19 혈장치료제 추가 생산 완료
- [코로나19 치료제 집중] 美 트럼프 대통령 코로나19 치료 타임라인
- GC녹십자, 코로나19 혈장치료제 국내 환자 첫 투여
- 국내 감염내과 교수가 평가한 코로나19 혈장치료는?
- 급여 확대된 코로나19 약제, 작년 3월 이후 처방 급감
- 렘데시비르 등 코로나19 약물치료 임상진료지침 개발
- 녹십자 혈장치료제, 중증에서 경증으로 임상설계 변경 권고

