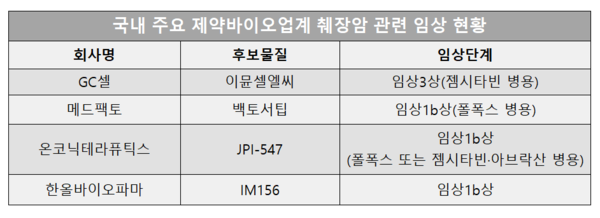
GC셀, 이뮨셀엘씨∙젬시타빈 병용 임상3상 진행 중
한올∙제일 임상1b상 중... 메드팩토 ‘백토서팁’, 췌장암에서도 가능성

[메디칼업저버 손형민 기자] 췌장암의 생존율을 높일 수 있는 치료제가 개발될 수 있을까?
췌장암은 최근 국내 5년 상대생존율은 13.3%에 그칠 정도로 치료성적이 좋지 않지만, 위치상 우리 몸 깊숙한 곳에 있어 발견도 어렵고 치료제도 부족한 실정이다.
여기에 도전장을 내민 국내 제약사들이 있다. GC셀, 한올바이오파마, 제일약품 자회사인 온코닉테라퓨틱스, 메드팩토가 그 주인공.
이들 제약사는 현재 임상 시험에서 상용화 가능성을 확인하고 있다. 치료제가 부족한 췌장암에 효과를 발휘할 수 있는 국내사의 치료제가 등장할지 기대가 모아지고 있다.
국내사, 희귀의약품 지정, 임상3상 진행 등 유의미한 성과 거둬
췌장암 치료 성적은 다른 암과 비교해 특히 나쁜 실정이다. 1993~1995년 대비 2014~2018년 암 발생자 생존율은 폐암의 경우 2배가량 높아져 최근 30%를 넘었다. 간암, 갑상선암, 위암 모두 최근 생존율이 과거보다 상승했다.
췌장암 5년 생존율이 예전과 비교해 많이 높아졌다지만 14% 정도에 불과하다. 췌장이 워낙 몸속 깊은 곳에 있어 검진을 통해서도 잘 발견되지 않으며, 발견돼도 4기 이상으로 치료 어려운 상황에 놓여져 있어서다.
이처럼 미충족 의료 수요가 큰 만큼 효과적인 신약 개발을 위한 노력도 이어지고 있다. 특히 국내 제약바이오 기업들이 잇따라 췌장암 치료제에 도전장을 내밀며 희귀의약품 지정, 임상3상 진행 등 유의미한 성과를 거두고 있다.
가장 상용화가 가까운 의약품은 GC셀 이뮨셀엘씨(성분명 엘씨자가혈액유래티림프구)다. 이뮨셀엘씨는 지난 2007년 승인받은 간세포암 제거술 후 종양제거가 확인된 환자에게 보조요법제로 투여할 수 있는 세포치료제다.
시장조사기관 아이큐비아에 따르면 지난해 293억원 판매실적을 올리는 등 현재 국내 세포치료제 중 매출 1위를 기록하고 있다.
GC셀은 면역세포치료제인 이뮨셀엘씨의 적응증을 확장하기 위해 노력해왔으며 그 결과 이뮨셀엘씨를 췌장암 치료제로 허가받기 위한 상업 임상을 결정했다.
해당 회사는 췌장암 표준치료제로 사용되는 젬시타빈 단독요법과 이뮨셀엘씨·젬시타빈 병용요법군 간 유효성과 안전성을 비교하는 임상3상시험계획(IND)을 식품의약품안전처로부터 지난 9월 승인받았다.
메드팩토는 골육종 치료제로 개발하는 백토서팁을 췌장암 치료제로 개발하기 위한 노력을 하고 있다.
회사 측은 폴폭스(류보코린∙플루오우라실∙이리노테칸∙옥살리플라틴)과 병용 임상1b상 중간 데이터를 미국암학회 연례학술대회(AACR 2022)에서 공개해 주목받기도 했다.
해당 임상에서 백토서팁 병용요법은 객관적 반응률(ORR) 23.1%, 전체생존기간 중앙값(mOS) 9.3개월로 기존 치료법과 비교해 치료 효과가 있음이 확인됐다.
한올바이오파마는 미국에서 췌장암 치료제를 임상 중이다. 회사 측에 따르면 지난 22일 미국 관계사인 이뮤노멧테라퓨틱스가 췌장암 치료제 후보물질인 ‘IM156’ 임상1b상에서 첫 환자 투약을 마쳤다.
IM156은 지난 해 2월 특발성 폐섬유화증에 이어 올 10월 미국식품의약국(FDA)로부터 췌장암에 대한 희귀의약품으로 지정된 바 있다.
해당 후보물질은 종양세포의 대사 기능과 근섬유아세포의 형성을 조절해 암 및 섬유증을 치료하는 대사항암제다. 암세포의 성장에 필요한 에너지원을 차단해 암세포를 선택적으로 제거하는 것을 목표로 한다.
이번 임상은 텍사스 대학교 MD 앤더슨 암센터 Shubham Pant 교수 주도로 진행되며, 진행성 췌장암 환자 25명 대상 IM156의 안전성과 유효성을 확인한다. 주요 목표점으로는 약물 안전성과 내약성을 평가하고 주요 목표점으로는 ORR, 무진행생존(PFS), OS 등이 포함됐다.
제일약품의 자회사 온코닉테라퓨틱스는 국내에서 췌장암 치료후보물질 'JPI-547'의 임상1b상을 진행 중이다. JPI-547은 PARP와 탄키라제(Tankyrase)를 억제하는 이중저해 표적 항암제다.
PARP 단백질은 DNA 복제 과정에서 발생하는 손상을 리페어 하는 효소다. 탄키라제는 ‘PARP-5’로, PARP 패밀리 중 하나다. WNT, YAP, AKT 등 종양 발생 경로와 연관돼 있다.
JPI-547은 두 효소를 모두 억제해 암세포의 증식을 멈추고 나아가 사멸시키도록 설계됐다.
해당 약물은 지난해 3월 FDA, 6월 식약처로부터 개발단계 희귀의약품으로 지정받기도 했다. 회사 측은 이번 임상에서 'JPI-547'과 폴폭스요법 또는 젬시타빈·아브락산 병용투여 후 안전성과 유효성을 평가할 계획이다.
관련기사
- 한올 관계사 이뮤노멧, IM156 임상1b상 투약 개시
- 췌장암 완치 가능하지만 '3명 중 1명' 치료 포기
- 대사증후군과 췌장암 발생 위험 상관관계 규명돼
- 온코닉테라퓨틱스, 260억원 시리즈B 투자 유치
- 한올, 전국 약대생 대상 아이디어 공모전 우수작 시상
- 췌관 선암 표준 치료요법, 10년 만에 바뀌나
- 췌장암은 여전히 난공불락 ... 그럼에도 조금씩 진전
- K-바이오, AACR 대거 출사표...신약후보물질 탐색 활발
- First-in-Class 외치는 국내 제약, 희귀의약품 개발도 앞장
- 메드팩토 백토서팁, 3개 암종서 도전장...성과 가시화

