영국 바이오뱅크 연구 결과, 치료제 없다면 Lp(a) 반복 검사 유용하지 않아
Lp(a) 치료 후보물질 임상단계…팰라카르센·올파시란·SLN360 주목
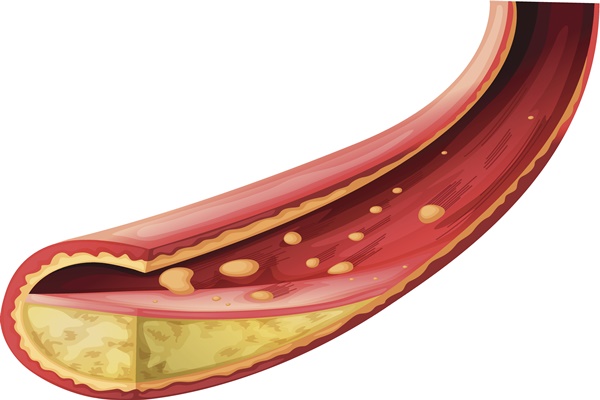
[메디칼업저버 박선혜 기자] 잔여 심혈관질환 위험을 낮추기 위한 치료 목표로 지질단백질(a)(Lp(a))이 학계의 주목을 받고 있다.
Lp(a)는 심혈관질환 발생과 연관된 유전적 위험요인이다. 출생 시 결정되며 식이요법 또는 운동으로 조절할 수 없고 변동 폭이 작아 일정 수준으로 유지된다.
2019년 유럽심장학회(ESC)·동맥경화학회(EAS)는 심혈관질환 위험을 확인하기 위해 평생 최소 1회 Lp(a)를 측정하도록 권고했다.
유전적으로 180mg/dL 이상의 높은 Lp(a)는 이형접합 가족성 고콜레스테롤혈증과 심혈관질환 위험이 유사하다고 판단한 것으로, 치료 목표는 50mg/dL 미만으로 제시했다.
이런 가운데 심혈관질환 위험을 평가하고자 일정 시간을 갖고 Lp(a)를 여러 번 검사하는 것이 유용할지 분석한 결과가 JACC 2월호를 통해 발표됐다(J Am Coll Cardiol 2022;79(7):617~628).
결과적으로, Lp(a)를 크게 낮출 수 있는 치료제가 없다면 Lp(a) 반복 검사의 혜택은 없었다.
Lp(a) 높은 성인, ASCVD 위험 1.29배↑
Lp(a)는 죽상경화성 심혈관질환(ASCVD)의 독립적인 위험요인으로 평가된다.
다인종 동맥경화 연구(MESA)에 등록된 무증상 성인 4512명을 조사한 결과, Lp(a)가 높다면 ASCVD 위험은 1.29배 유의하게 상승했다(J Am Coll Cardiol 2022;79(8):757~768).
게다가 Lp(a)가 높지 않고 관상동맥칼슘(CAC) 점수가 0점인 성인과 비교해 Lp(a)가 높고 CAC 점수가 100점 이상인 성인의 ASCVD 위험은 4.71배 높은 것으로 나타났다.
즉 이번 결과는 Lp(a)가 높다면 ASCVD 위험이 증가할 수 있으므로, 검사를 통해 Lp(a) 농도를 확인하고 이를 ASCVD 위험 평가에 반영해야 한다는 것을 시사했다.
Lp(a) 낮추는 치료제 없다면, 평생 1회 측정 충분
유럽 가이드라인에서는 심혈관질환의 독립적 위험요인인 Lp(a)를 평생 최소 1회 측정하도록 권고한다.
그러나 시간에 따른 Lp(a) 변동성은 잘 알려지지 않았고 반복 검사를 통해 관상동맥질환 위험 예측도를 개선할 수 있는지도 명확하지 않다.
JACC 2월호에 실린 영국 바이오뱅크 분석 연구에서는 참가자 1만 6017명의 데이터베이스를 바탕으로 반복된 Lp(a) 측정 값의 안정성을 조사하고, Lp(a) 몰농도(molar concentration)의 불안정성과 관상동맥질환 발생 간 연관성을 평가했다.
그 결과, 등록 당시부터 추적관찰 4.42년(중앙값) 후 Lp(a) 몰농도는 거의 변화가 없었다. 추적관찰 기간을 3년 미만, 3~4년, 4~5년, 5년 이후 등으로 세분화해 평가해도 등록 당시와 측정 기간 사이의 Lp(a) 몰농도는 안정적이었고 큰 변화가 관찰되지 않았다.
단, 추적관찰한 Lp(a) 몰농도가 120nmol/L라면 관상동맥질환 발생 위험은 1.32배 유의하게 증가했다.
이번 결과에 따라 전문가들은 Lp(a)를 효과적으로 낮추는 치료제가 등장하지 않는다면 Lp(a)를 반복 측정하지 않아도 된다는 데 중지를 모은다. 즉, Lp(a) 농도를 크게 낮추는 치료제가 개발된다면 검사에도 변화가 나타날 수 있다는 것이다.
연구 교신저자인 미국 매사추세츠 종합병원 Pradeep Natarajan 박사는 "관상동맥질환 발생을 예측할 때 추적관찰한 Lp(a) 농도는 등록 당시 평가를 넘어서는 추가 정보를 제공하지 못했다"며 "Lp(a)를 현저하게 낮추는 치료제를 투약하지 않는다면, 심혈관질환이 없는 환자에게 반복된 Lp(a) 검사는 등록 당시 평가 이상의 혜택을 제공하지 않을 것"이라고 밝혔다.
연구 1저자인 캐나다 브리티시 컬럼비아대학 Mark Trinder 교수는 "이번 결과는 Lp(a)를 실질적으로 변화시키는 치료제가 없다면, 정확한 Lp(a) 몰농도 1회 측정이 ASCVD 위험을 평가하는 데 효율적임을 시사한다"고 밝혔다.
명지병원 조윤형 교수(심장내과)는 "Lp(a)는 유전적으로 이미 결정된 심혈관질환 위험요인으로, 1회 검사만으로 의미 있는 값을 얻을 수 있다"며 "Lp(a)를 낮추는 치료제가 개발된다면 치료 전후 Lp(a) 수치를 비교하기 위해 검사를 최소 2회 할 수 있을 것으로 예상한다. 그러나 확실한 치료제가 없는 상황에서 심혈관질환 위험만 평가하기 위해서라면 Lp(a)는 평생 1회 측정만으로 충분하다"고 강조했다.
Lp(a) 표적 치료 후보물질 개발 단계
노바티스 '팰라카르센', 임상3상 환자 등록 순항 중
이에 따라 Lp(a) 검사에 변화를 줄 수 있을 것으로 전망되는 Lp(a) 표적 치료 후보물질에 관심이 쏠린다.
가장 앞서 있는 기대주는 노바티스의 팰라카르센(AKCEA-APO(a)-LRX)이다. 펠라카르센은 안티센스 올리고핵산(ASO) 기반 치료제다.
임상2상 결과, 팰라카르센은 용량 의존적으로 Lp(a)를 최대 80%까지 낮췄고 심각한 이상반응은 보고되지 않았다.
이를 근거로 진행되는 HORIZON 임상3상은 순항 중이다. 임상3상의 목표 모집 환자 수는 7680명이며, 지난해 8월 기준 절반가량 등록한 것으로 알려졌다.
학계에서는 HORIZON 결과에 따라 Lp(a)를 치료 목표로 둬야 할지 재논의해야 할 것이라는 목소리가 나온다. 연구는 2025년 5월 종료될 예정이다.
암젠 '올파시란', 임상1상서 Lp(a) 90% 이상 낮춰
암젠과 미국 애로우헤드 파마슈티컬스가 개발 중인 올파시란(AMG890)도 새로운 Lp(a) 치료제로 기대를 모은다. 올파시란은 GalNAc 접합기술을 활용한 siRNA 치료제다.
2020년 발표된 올파시란 임상1상 결과, 1회 피하주사 시 Lp(a)가 90% 이상 감소했다. 또 9mg/kg 이상 투여 시 효과가 6개월 이상 지속됐다.
가장 흔한 치료 관련 이상반응(TEAE)는 두통(올파시란군 10% vs 위약군 25%), 상기도감염(15% vs 13%)이었다. 올파시란군에서 우려할만한 안전성 문제는 감지되지 않았다.
이에 2020년 7월 올파시란 임상2상이 시작됐다. 이중맹검 무작위 위약 대조 임상2상에서는 올파시란 피하주사 시 등록 당시 대비 Lp(a) 변화를 평가하고 이를 위약과 비교한다. 연구는 내년 3월 종료될 것으로 보인다.
사일런스 테라퓨틱스 'SLN360', ACC서 임상1상 공개 예정
또 다른 siRNA 치료제인 영국 사일런스 테라퓨틱스의 SLN360도 두 치료제의 뒤를 바짝 쫓고 있다.
SLN360은 간세포의 LPA 유전자로부터 전사된 mRNA를 표적하고 침묵(silence)시키기 위해 체내 자연적인 RNA 간섭 과정을 활용해 Lp(a) 생성을 줄이도록 만들어진 siRNA 치료제다.
SLN360의 APOLLO 임상1상은 Lp(a) 농도가 최소 150nmol/L이고 심혈관질환이 없는 32명을 대상으로 진행됐다. 이들은 SL360 30mg, 100mg, 300mg 이하, 600mg 이하 또는 위약 등 단일 피하주사군에 배정됐다. 추적관찰은 최대 150일 동안 시행됐다.
탑라인 결과, SLN360은 용량 의존적으로 Lp(a)를 46%에서 최대 98%까지 크게 낮췄다. 개발사에 의하면 150일 동안 Lp(a)는 최대 81% 감소가 유지됐다.
안전성 평가에서 낮은 등급의 이상반응인 주사부위 반응이 가장 두드러지게 발생했고 주로 고용량 투여 시 나타났다. 임상적으로 중요한 안전성 문제는 나타나지 않았다.
APOLLO 임상1상의 자세한 결과는 4월 열리는 미국심장학회 연례학술대회(ACC 2022)에서 공개될 예정이다.

