알테오젠·브릿지바이오 등 기술수출로 잭팟...신라젠·헬릭스미스 '반면교사'
기술수출로 글로벌 제약사 임상 노하우 축적 "선순환 구조 밑거름될 것"

[메디칼업저버 양영구 기자] 국내 제약·바이오 업계가 임상에서 고배를 마시면서 고전한 가운데 기술수출이 재차 주목받고 있다.
글로벌 임상에 도전하기에는 아직까지 자금력이 부족한 우리나라 업계 환경 안에서는 기술수출을 통해 기반을 다져 세계 무대에 도전해야 한다는 자성도 나온다.
'임상실패' 리스크 컸던 K-바이오
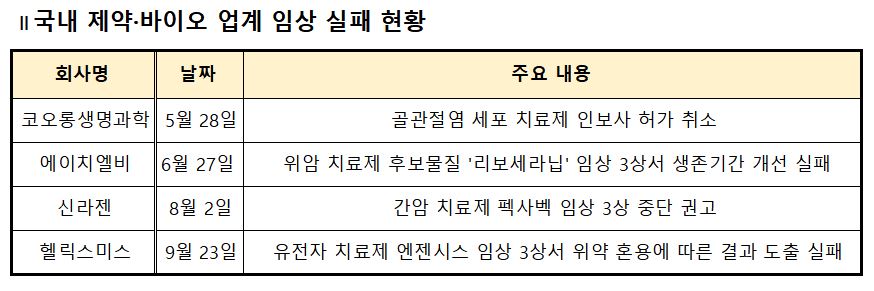
의약품 상용화의 마지막 단계인 임상 3상은 일반적으로 약 3000억원에 육박하는 비용이 필요한 것으로 알려져 있다.
후보물질 단계부터 임상 3상까지 개발을 이어온 것도 중요하지만, 이 단계에서 가장 많은 비용이 필요한 만큼 3상 실패라는 리스크는 회사의 존립을 위협하기도 한다.
올 한 해 K-바이오에 회의론이 제기됐던 이유도 여기서 출발한다. 무리하게 임상 3상을 진행하며, 실패라는 리스크를 떠안은 게 결정적이었다.
실제로 코오롱생명과학은 인보사의 성공을 위해 임상을 무리하게 추진, 주성분이 뒤바뀌는 결과를 낳았다.
특히 무리한 임상 진행에 따른 실패는 바이오 업계가 두드러졌다.
에이치엘비는 개발 중인 위암 치료제 후보물질 리보세라닙 임상 3상(ANGEL) 결과, 진행성 위암 환자의 전체 생존기간 개선에 실패했다.
신라젠은 펙사벡의 간암 환자 대상 임상 3상(PHOCUS)의 무용성 평가 결과, IDMC(Independent Data Monitoring Commitee, 독립적 데이터 모니터링 위원회)로부터 임상 중단을 권고받았다.
최근에는 헬릭스미스의 유전자 치료제 엔젠시스의 임상 3상 과정에서 시험약과 위약을 혼합투여하면서 결과를 도출하지 못하는 사태도 겪었다. 위업계 한 관계자는 "경험이 부족하더라도 기초적인 부분조차 관리하지 못하는 상황에서 신약을 개발할 수 없다"며 "임상은 의약품 개발을 위한 것이지, 주가 부양을 위한 것은 아니다"고 일갈했다.
다시 주목받는 '기술수출'
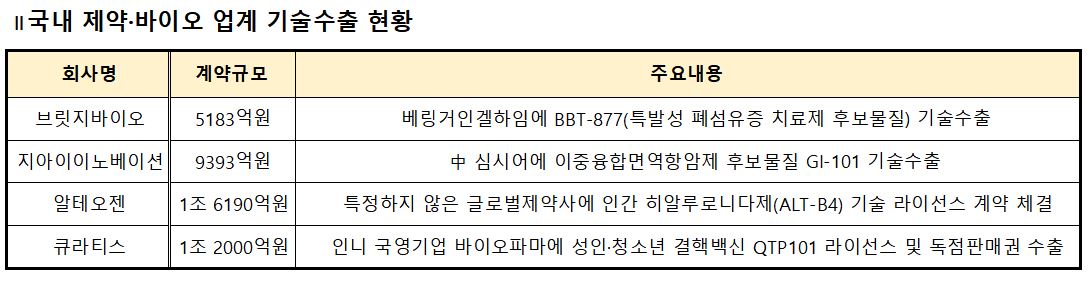
제약·바이오 업계가 올 한해 총 4조원 규모의 기술수출 계약에 성공하면서 다시금 주목받고 있다. 잇따른 임상 3상 실패에 따른 불신을 반전한 셈이다.
지난 7월 브릿지바이오테라퓨틱스는 베링거인겔하임에 특발성 폐섬유증 치료 후보물질 BBT-877을 11억 4500만유로(약 5183억원)에 기술수출 계약을 체결했다. 이번 기술수출은 후보물질 도입 후 약 2년 만으로, 단일 화합물 기준 국내 업계 사상 최대 규모다.
지아이이노베이션은 중국 제약사 심시어와 이중융합면역항암제 GI-101의 중국 지역 독점개발 권리를 7억 9600만달러(약 9393억원)에 기술이전 계약을 체결했다. GI-101은 지아이이노베이션이 보유한 이중융합단백질 개발 기반기술 GI-SMART 플랫폼을 이용해 만든 면역항암제다.
알테오젠은 10대 글로벌 제약사(미특정)와 정맥주사(IV) 제형을 피하주사(SC) 제형을 변환해주는 인간 히알루로니다제(ALT-B4) 기술에 대한 비독점적 글로벌 라이선스 계약을 따냈다.
반환 의무가 없는 계약금은 1300만 달러(약 153억원)이며, 개발 단계별 마일스톤을 합한 총 계약규모는 13억7300만 달러(약 1조6190억원)에 달한다.
이와 함께 바이오벤처 큐라티스는 인도네시아 국영기업인 바이오파마에 성인·청소년 결핵백신 QTP101의 라이선스와 독점판매권을 1조 2000억원에 제공하는 계약을 체결했다.
기술수출은 계약금이라는 금전적 이익 이외에 글로벌 제약사와 공동으로 임상을 진행하며 배울 수 있는 장점이 있다. 물론 기술이전을 받은 글로벌 제약사가 임상을 진행하지만, 이 과정에서 이전 데이터가 반드시 필요한 만큼 협업하지 않을 수 없는 구조다.
실제 최근 미국식품의약국(FDA)으로부터 시판허가를 따낸 SK바이오팜의 뇌전증 치료제 엑스코프리는 미국 재즈파마슈티컬에 기술이전한 수면장애 신약 수노시에 대한 공동연구를 진행하며 습득한 결과물로 알려져 있다.
제약·바이오 업계는 국내 환경의 선순환 구조를 만들기 위해서라도 무리하게 임상 3상에 도전하기보다는 기술수출 계약을 통한 선순환 구조의 기반을 만들어야 한다고 조언한다.
업계 한 관계자는 "그동안 국내 제약·바이오 업계는 자금력이 부족한 바이오벤처가 독자적으로 임상 3상을 진행하고, 전통 제약사가 기술수출에 집중하는 형태였다"며 "기술수출을 통해 배운 글로벌 제약사의 노하우를 접목한다면 전통제약사, 바이오 벤처 모두 독자적으로 임상을 진행할 수 있는 환경이 조성될 것"이라고 말했다.
