식약처, 15일 불면증 치료제 앱 에임메드 ‘솜즈’ 국내 허가
6~9주간 실시간 피드백∙교육훈련 프로그램으로 맞춤형 불면증 치료 가능
이유진 교수 “인지행동치료를 앱으로 구현해 편리…수가 논의는 시기상조”

[메디칼업저버 손형민 기자] 국내 디지털 치료제 1호 품목으로 허가된 불면증 치료제 앱 솜즈(Somzz)가 수가 등의 과제를 해결하며 상용화까지 성공할 수 있을지 귀추가 주목된다.
식품의약품안전처는 15일 에임메드의 불면증 증상 개선 소프트웨어 솜즈를 국내 첫 디지털 치료제로 허가했다.
이는 디지털 치료제의 큰 획을 긋는 것이라고 평가된다. 그간 확증임상을 통해 허가에 임박 품목들이 대거 있었지만, 실제 허가된 것은 솜즈가 첫 사례이기 때문이다.
솜즈는 불면증 환자를 치료하는 표준요법인 불면증 인지행동치료법(CBT-I)을 ‘모바일 앱’으로 구현한 소프트웨어 의료기기다.
해당 제품은 6~9주간 실시간 피드백, 행동중재 및 교육훈련 프로그램으로 환자 맞춤형 불면증 치료를 제공한다.
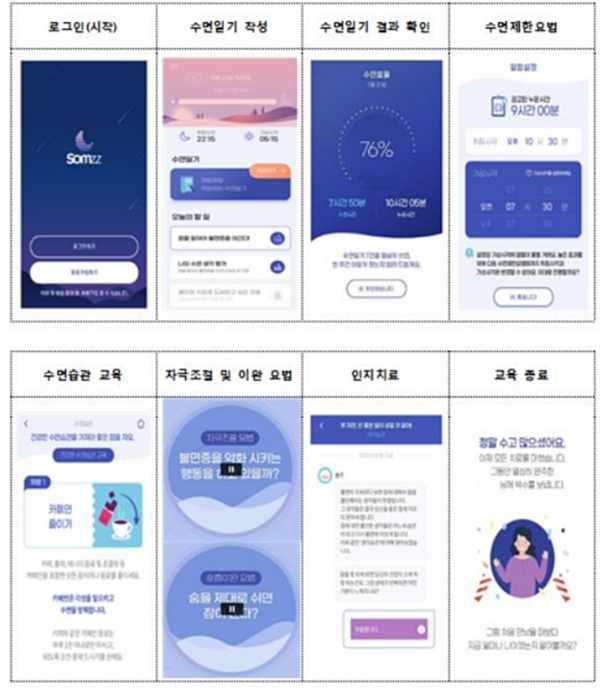
불면증 환자가 의료기관을 방문해 솜즈를 처방받으면 잠드는 시각, 일어난 시각 등을 기입할 수 있는 수면일기를 통해 실시간 피드백이 가능하다.
또 솜즈는 수면습관교육, 자극 조절 및 이완 요법 등을 통해 환자가 불안감을 느끼지 않도록 다양한 프로그램을 제공한다.
식약처는 솜즈의 치료 효과를 검증하기 위해 에임메드가 6개월간 서울대병원, 삼성서울병원, 고대안암병원에서 실시한 임상 시험 결과를 검토했다.
임상 결과, 솜즈 사용 전과 사용 후 '불면증 심각도 평가척도'에서 통계적으로 유의미한 개선이 확인됐다.
식약처는 "정신건강의학과, 가정의학과 등 전문가로 구성된 의료기기위원회를 개최해 안전성과 유효성이 확보됐음을 자문받았으며 과학적이고 철저한 심사를 거쳐 허가했다"고 덧붙였다.
솜즈 임상을 진행한 서울대병원 이유진 교수(정신건강의학과)는 "솜즈는 잠이 들기 어렵거나, 중간에 깨거나 아침에 예상보다 일찍 깨는 증상이 주 3회 이상 3개월 이상 지속돼 일상생활에 장애를 받는 만성 불면증 환자가 처방 대상"이라며 "불면증 치료에는 수면제가 주로 쓰이지만, 가장 좋은 치료는 인지행동치료다. 해당 치료는 일주일에 한 번씩 6~8주 정도 병원을 방문해야 해 접근성이 떨어진다. 솜즈는 이런 인지행동치료를 앱으로 옮겨 놓은 것이어서 활용 가능성이 높다"고 말했다.
이어 "만성 불면증 환자는 초기에 수면제와 같은 약물치료를 병행하다가 약을 줄이거나 끊고 대부분 인지행동치료로 넘어간다. 이런 불면증 치료를 앱으로 쉽게 접근할 수 있다는 점에서 의의가 있다"고 덧붙였다.
현재는 솜즈 사용 시 6~9주 동안 추적 관찰 후 다시 병원에 방문해야 하는 등의 구체적 수칙은 정해지지 않았다. 또 환자가 앱을 실행하지 않을 경우 치료가 어려운 부분도 간과할 수는 단점도 있다.
이에 대해 이 교수는 "아직 구체적으로 정해진 것은 없지만 솜즈의 효과 확인 등을 주치의와 상의하기 위해서 병원에 다시 방문해야 하지 않을까 생각한다"며 "접근성을 높이기 위해 앱을 깔아놓고도 실행하지 않으면 치료가 어렵다. 실제 인지행동치료를 진행할 때도 시간적인 여유가 앖어 병원에 방문하지 못하는 경우가 많다. 앱 푸쉬 알람 기능이 순응도를 올리는 데 도움 될 것"이라고 전했다.
솜즈 수가 논의까지는 아직...'리얼월드 데이터 확보해야'
솜즈가 국내 디지털 치료기기로 첫 허가가 되면서 디지털 치료제의 혁신 기술이 상용화될 수 있다는 가능성에 큰 첫발을 내디뎠다는 나온다.
현재 국내에서는 웰트∙하이 등 6개 회사가 불면증과 불안 장애, 알코올 사용 장애 등 여러 디지털 치료 기기 임상 시험을 진행 중이다.
디지털 치료제 개발 후발사들은 솜즈가 개척할 수가, 보험급여 트랙 등을 눈여겨 보고 있다.
국내 디지털 치료제 1호인 솜즈가 어떤 수가를 받느냐에 따라 2호, 3호로 등장할 디지털 치료제에도 지대한 영향을 끼칠 가능성이 높기 때문이다.
현재 유력하게 거론되는 것은 사용량-약가 연동제다. 디지털 치료제가 국내 처음 선보이는 것이라 사용량 예상이 어렵다. 따라서 예상 사용량 보다 많은 경우 가격을 인하, 예상 사용량보다 실사용자가 적을 때 가격 인상을 할 것으로 보인다.
다만, 이 교수는 솜즈의 보험급여나 수가 논의는 아직 섣부르다는 의견을 밝혔다.
이 교수는 "솜즈는 현재 수가를 말하기 어려울 정도로 초기 단계라고 봐야 한다"며 "혁신 의료기술이 수가를 받기 위해서는 신규 기술에 등재 돼야 한다. 현재까지 솜즈는 혁신의료기기로 지정된 상황"이라고 말했다.
이어 "현재 단계에서는 연구 목적이라든지, 일부 환자에게 리얼 월드 데이터를 모으기 위해 솜즈를 사용할 수 있다. 그런 데이터가 더 모여서 신규 기술에 등재할 수 있는 근거를 모아야 한다. 이는 앞으로 2~3년이 걸릴 수도 있다"며 "얼마만큼의 절차를 확인할 것인지 앞으로 논의가 필요하다. 장기적으로 봐선 수가, 보험급여에 진입해 많은 불면증 환자가 도움을 받았으면 좋겠다"고 덧붙였다.

