[WCLC 2022] GEMSTONE-301 임상3상, 최종 무진행 생존 분석 결과 발표
수게말리맙, 동시·순차적 항암화학방사선요법 이후 효과적이고 안전

[메디칼업저버 박선혜 기자] 중국 시스톤 파마슈티컬사의 항PD-L1 단클론항체 수게말리맙이 절제 불가능한 3기 비소세포폐암(NSCLC) 환자의 공고요법으로 입지를 다졌다.
GEMSTONE-301 임상3상 결과, 동시 항암화학방사선요법(cCRT) 또는 순차적 항암화학방사선요법(sCRT)을 받은 이후 질병 진행이 없는 절제 불가능한 3기 NSCLC 환자에게 공고요법으로 수게말리맙 투약 시 생존 혜택을 얻을 수 있었고 안전했다.
이번 연구 결과는 6~9일 오스트리아에서 온·오프라인으로 열린 국제폐암연구협회(IASLC) 개최 세계폐암학회 학술대회(WCLC 2022)에서 공개됐다.
중간분석 결과 긍정적…장기간 추적관찰 필요성 제기
GEMSTONE-301 임상3상은 항암화학방사선요법 이후 질병이 진행되지 않은 절제 불가능한 3기 NSCLC 환자를 대상으로 공고요법으로서 수게말리맙의 가능성을 평가한 연구다.
지난 2월에는 사전에 계획된 무진행 생존 중간분석 결과가 발표됐다(Lancet Oncol 2022;23(2):209~219). 지난해 3월 8일 데이터 컷오프 시점을 기준으로 평가한 무진행 생존기간은 수게말리맙군이 9.0개월로 위약군 5.8개월과 비교해 길었다.
수게말리맙이 무진행 생존기간을 통계적으로 유의하게 개선한다는 결과에 따라, cCRT 또는 sCRT 이후 질병이 진행되지 않은 절제 불가능한 3기 NSCLC 환자에게 수게말리맙을 공고요법으로 사용할 수 있다는 기대감이 높아졌다. 학계에서는 중간분석 결과를 토대로 장기간 추적관찰을 통한 효과 및 안전성 평가 필요성이 제기됐다.
무진행 생존기간, 수게말리맙군 10.5개월 vs 위약군 6.2개월
이번 학술대회에서는 GEMSTONE-301 임상3상의 무진행 생존에 대한 최종분석 결과가 베일을 벗었다. 연구에 모집된 총 381명 환자는 수게말리맙군과 위약군에 2:1 비율로 무작위 배정돼 24개월까지 치료받았다. 수게말리맙군은 3주마다 1200mg을 정맥주사했다.
전체 환자군은 △전신수행능력평가인 ECOG PS 점수(0단계 vs 1단계) △항암화학방사선요법 유형(cCRT vs sCRT) △총 방사선 선량(60Gy 미만 vs 60Gy 이상) 등에 따라 계층화됐다.
1차 목표점은 독립중앙심사위원회(BICR)가 평가한 무진행 생존으로 정의했다. 2차 목표점은 전체 생존, 연구자가 평가한 무진행 생존, 전체 반응률, 반응기간 등으로 설정했다. 추적관찰 기간(중앙값)은 수게말리맙군 27.1개월, 위약군 23.5개월이었다.
분석 결과, BICR이 평가한 무진행 생존기간(중앙값)은 수게말리맙군 10.5개월, 위약군 6.2개월로 수게말리맙군이 더 길었다. 이에 따른 무진행 생존 혜택은 수게말리맙군이 위약군 대비 35% 더 얻을 수 있었다(stratified HR 0.65; 95% CI 0.50~0.84).
기간별 무진행 생존율은 24개월에 수게말리맙군 38.6%와 위약군 23.1%, 36개월에 각 26.1%와 0%로 수게말리맙이 우월한 결과를 얻었다.
항암화학방사선요법 유형에 따른 무진행 생존 혜택도 앞선 결과와 유사하게 나타났다. 무진행 생존기간(중앙값)은 sCRT를 받은 환자군에서 수게맙리맙군 8.1개월과 위약군 4.1개월, cCRT를 받은 환자군에서 각 15.7개월과 8.3개월로 집계됐다.
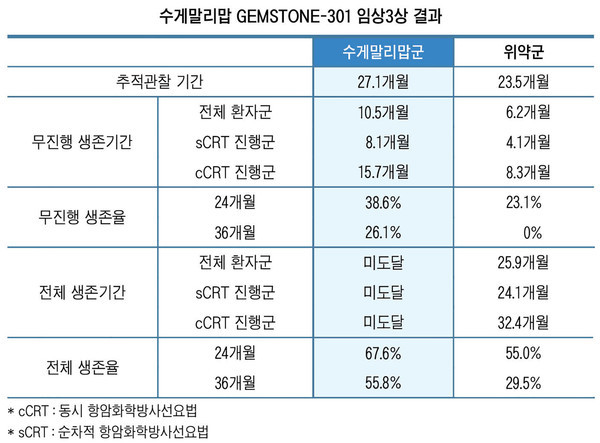
이어 전체 생존기간(중앙값)은 수게말리맙군의 경우 아직 도달하지 않았고 위약군은 25.9개월로 조사됐다. 항암화학방사선요법 유형에 따라서는 수게말리맙군은 전체 생존기간(중앙값)에 도달하지 않았지만 위약군은 sCRT를 받은 환자군에서 24.1개월, cCRT를 진행한 환자군에서 32.4개월로 집계됐다.
전체 생존율은 수게말리맙군은 33.3%, 위약군은 42.9%로 수게말리맙군의 사망 위험이 31% 유의하게 낮았다(HR 0.69; 95% CI 0.49~0.97). 기간에 따른 전체 생존율은 24개월에 수게말리맙군 67.6%와 위약군 55.0%, 36개월에 각 55.8%와 29.5%였다.
항암화학방사선요법 유형에 따른 전체 생존율은 24개월에 sCRT 진행 환자군에서 수게말리맙군 70.7%와 위약군 53.7%, cCRT 진행 환자군에서 각 66.3%와 57.6%로 조사됐다. 36개월에는 sCRT 진행 환자군에서 수게말리맙군 59.0%와 위약군 43.7%, cCRT 진행 환자군에서 각 54.1%와 19.8%였다.
안전성 평가에서 3등급 이상 치료 관련 이상반응 발생률은 수게말리맙군 11.4%, 위약군 5.6%로 확인됐다. 수게말리맙군에서 가장 흔하게 보고된 3등급 이상 치료 관련 이상반응은 면역 매개성 폐질환, 발진, 갑상선기능저하증, 폐렴 등이었고 위약군은 폐렴과 빈혈이 주로 나타났다.
연구를 진행한 중국 광둥성 인민병원 Yi-Long Wu 박사는 "최종 분석에서 수게말리맙 투약 시 지속적인 무진행 생존 혜택이 나타났고 내약성이 좋았다. 전체 생존에 대한 예비 데이터는 수게말리맙의 치료 혜택이 있음을 시사한다"며 "이번 결과는 수게말라맙이 cCRT 또는 sCRT 이후 질병 진행이 없는 절제 불가능한 3기 NSCLC 환자에게 안전하고 효과적인 공고요법이라는 근거가 된다"고 강조했다.

