인증절차, 신청 제출자료, 심사항목 등 담겨
[메디칼업저버 정윤식 기자] 식품의약품안전처가 혁신의료기기의 제품화 지원을 위해 혁신의료기기 소프트웨어(S/W) 제조기업을 인증하는 기준 및 절차를 마련했다.
혁신의료기기소프트웨어는 의료기기산업 육성 및 혁신의료기기 지원법(의료기기산업법)에 따라 정보통신기술, 바이오기술, 나노기술 등 첨단 기술을 적용해 기존 의료기기나 치료법에 비해 안전성 및 유효성을 개선했거나 개선할 것으로 기대되는 의료기기를 말한다.
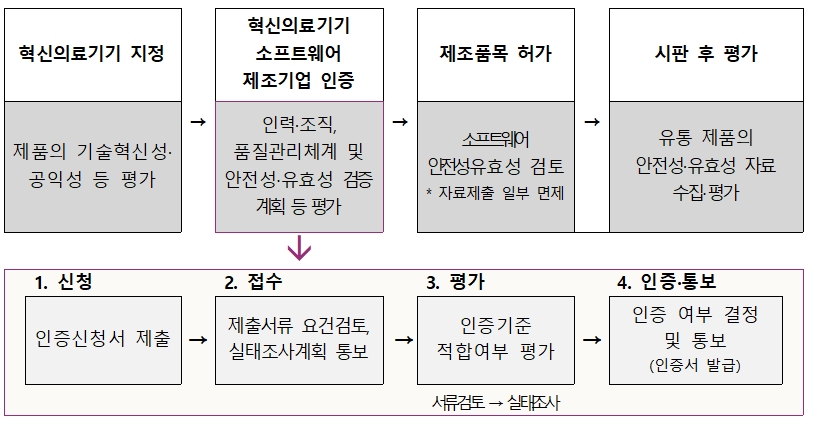
혁신의료기기소프트웨어 제조기업 인증은 혁신의료기기로 지정된 의료기기소프트웨어 제조업체의 연구개발 인력, 조직, 품질관리체계 등을 평가해 우수 제조기업을 인증하는 제도다.
제조허가 시 제출자료 일부를 면제하는 등 신속제품화를 위한 허가 특례를 지원하는 게 특징이다.
식약처는 의료기기 업체들이 인증 제도를 이해하고 적극 활용할 수 있도록 하기 위해 이번 안내서를 발간했다고 설명했다.
안내서의 주요 내용은 혁신의료기기소프트웨어 제조기업 인증에 필요한 △인증절차 △인증 신청 시 제출자료 △인증 세부 심사항목 등이다.
세부 심사항목은 △연구·개발 인력 △연구·개발 조직 △연구·개발 실적 △제조 및 품질관리체계 등 4개 분야로 나눠 각 분야에 대한 해당 기업의 우수성을 평가할 수 있도록 구성했다.
식약처 관계자는 "앞으로도 혁신의료기기 제품화를 촉진하고 의료기기산업의 경쟁력 강화를 위해 노력할 것"이라고 말했다.
관련기사
정윤식 기자
ysjung@monews.co.kr

