식약처, 변경허가·신고 받지 않고 첨가제 임의 사용 등 약사법 위반 확인
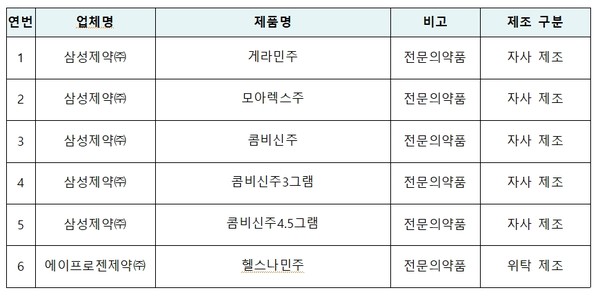
[메디칼업저버 정윤식 기자] 식품의약품안전처는 의약품 제조업체 삼성제약이 제조한 6개 품목(5개 자사, 1개 수탁)을 잠정 제조·판매 중지하고 회수 조치한다고 8일 밝혔다.
이번 조치는 의약품 GMP 특별 기획점검단이 삼성제약을 특별점검한 결과 △변경허가·신고를 받지 않고 첨가제 임의 사용 △제조기록서 거짓 작성 등 약사법 위반 사항을 확인한 데 따른 것이다.
식약처는 해당 6개 품목을 대체 의약품으로 전환하고 제품 회수가 적절히 수행될 수 있도록 의·약사 등 전문가의 협조를 요청하는 안전성 속보를 배포했다.
아울러 보건복지부와 건강보험심사평가원에 병·의원에서 해당 품목을 처방하지 않도록 조치해 줄 것을 요청했다.
식약처 관계자는 "앞으로도 의약품 GMP 특별 기획점검단을 운영해 의약품 제조소에 대한 불시 점검을 연중 실시하는 등 환자 안전을 최우선으로 고려하고 필요한 조치를 신속하게 할 것"이라고 말했다.
관련기사
정윤식 기자
ysjung@monews.co.kr

