대상포진 및 구순포진 치료제…유럽 의약품안전관리기구 안전성 정보 검토
국내 23품목 시판…식약처, 사용상 주의사항 허가내용 변경 의견조회 중
[메디칼업저버 정윤식 기자] 발라시클로비르(Valacyclovir) 성분 경구제에서 'DRESS 증후군(Drug reaction with eosinophilia and systemic symptoms syndrome)'이 보고돼 허가내용 변경이 추진된다.
발라시클로비르를 주성분으로 국내에 시판되는 경구 약제 품목은 23개로, 이 약제는 대상포진 치료를 비롯해 성기포진 감염증 재발·전염 억제, 신장이식 후 거대세포바이러스 감염 예방, 구순포진 치료, 소아 수두 치료 등에 사용하도록 허가됐다.
이들 품목의 국내 처방 규모는 2020년 기준 145억원가량으로 추산되며 특히, 글락소스미스클라인(GSK)의 발트렉스가 점유율 40%를 차지하고 있다.
최근 식품의약품안전처는 유럽의약품안전관리기구(HMA)의 발라시클로비르 성분 제제에 대한 안전성 정보를 검토한 결과 DRESS 증후군이 보고됐다고 밝혔다.
DRESS 증후군은 약물에 의한 알레르기 반응의 일종이다.
발열과 피부발진이 생기고 혈액에서 호산구가 증가하거나 비전형 림프구가 관찰되며, 급성 간염 및 신부전 등 내부 장기에 영향을 미쳐 심할 경우 사망에도 이를 수 있다.
이에 식약처는 국내에서 시판되는 발라시클로비르 성분 의약품에 대한 허가사항 변경안을 마련하고 의견조회 중이다.
변경안에 따르면 발라시클로비르 단일제(경구제)의 '사용상의 주의사항' 중 이상반응 항목과 일반적 주의사항 항목에 새로운 내용이 추가된다.
우선, 이상반응 항목에는 '빈도불명 호산구 증가와 전신증상을 동반한 약물반응(DRESS)'이라는 표현이 신설된다.
이어 일반적 주의사항 항목에서 '생명을 위협하거나 치명적일 수 있는 DRESS 증후군이 이 약 치료와 연관해 보고됐다'고 서술하고 있다..
아울러 △환자들은 처방 받을 시 피부 반응의 징후와 증상에 대한 권고를 들어야하며 환자에 대해 면밀히 모니터링을 해야한다 △DRESS 증후군을 시사하는 징후와 증상 발생 시 이 약의 치료를 즉각 중단하고 대체 치료를 고려해야 한다 △사용 시 환자에게 DRESS 증후군이 발생한 경우, 어떠한 시점에도 이 약의 치료를 개시해서는 안 된다 등의 문구가 새롭게 삽입됐다.
현재 발라시클로비르를 성분으로 대상포진 치료 목적의 경구제를 국내 시판하고 있는 업체는 총 23곳이다.
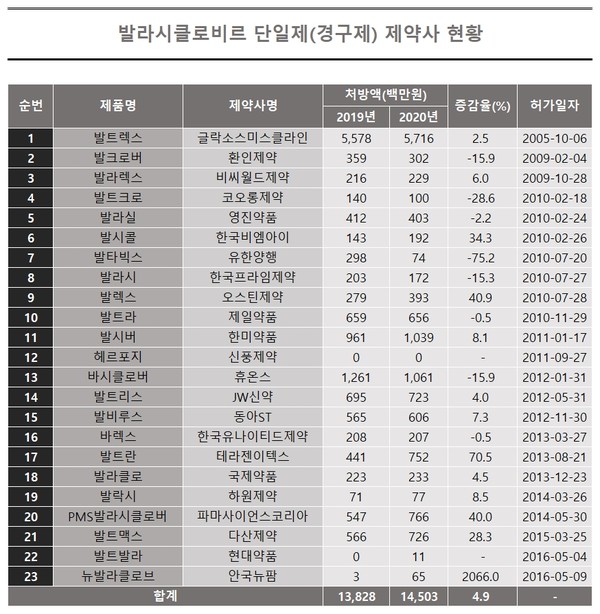
GSK, 휴온스, 환인제약, 유한양행, 한국프라임제약, 제일약품, 한미약품, 동아에스티, 한국유나이티드제약, 현대약품 등이며 이중 GSK의 처방 규모가 가장 크다.
실제로 GSK의 발트렉스는 지난해 57억 1600만원의 처방 실적을 올렸는데, 이는 전체 규모인 145억원의 40%에 달한다.
발트렉스는 2000년부터 2016년까지 동아제약을 통해 독점 판매가 이뤄지다가, 2017년 2월부터 GSK가 직접 판매에 뛰어들었다.
휴온스의 바시클로버(10억 6100만원)와 한미약품의 발시버(10억 3900만원)가 발트렉스의 뒤를 잇고 있지만 이들의 처방규모는 발트렉스의 5분의 1 수준이다.
발시버만 전년 대비 8.1% 처방액이 상승한 수치고, 바시클로버는 15.9% 감소했다.
발라시클로비르 성분 의약품의 지난해 전체 처방 규모는 2019년에 비해 4.9%가량 성장했다(138억원→145억원).
하지만 환인제약, 코오롱제약, 유한양행, 한국프라임제약 등 일부 제약사의 제품은 처방이 감소세인 것으로 확인된다.
한편, 발라시클로비르 성분의 DRESS 증후군 보고와 관련된 이번 변경안에 대한 전문가 및 협회 등의 검토 의견은 오는 15일까지 식약처 의약품안전평가과에서 접수하고 있다.


표가 맞나요? 내용이 맞나요