지난 4월 재심의 판정 후 3개월 만에 약평위 문턱 통과
HLB제약 씨트렐린, 평가금액 이하 수용 조건부 통과
[메디칼업저버 김지예 기자] 허가-평가-협상 병행 시범사업의 1호 약제 중 하나인 입센의 빌베이(성분명 오데빅시바트1.5수화물)가 재심 끝에 급여 적정성을 인정받았다.
건강보험심사평가원은 10일 올해 제7차 약제급여평가위원회를 열고 이같이 심의했다고 밝혔다.
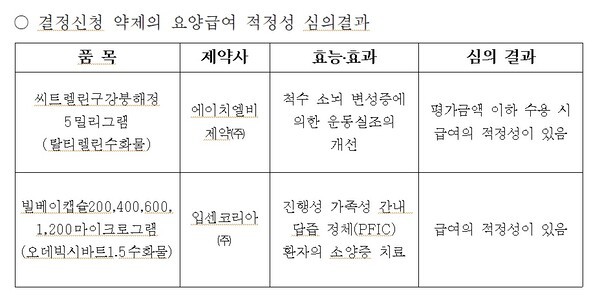
이날 약평위는 진행성 가족성 간내 답즙 정체증(PFIC) 환자의 소양증 치료를 적응증으로 한 빌베이캡슐 200·400·600·1200μg의 급여 적정성을 인정했다.
빌베이는 혁신의약품의 급여 등재 기간을 단축하기 위한 허가-평가-협상 병행 시범사업 1호 약제로, 식품의약품안전처-심평원-국민건강보험공단의 심사가 동시에 진행되며, 빠른 급여화가 기대됐던 약제다.
그러나 지난 4월 약평위에서 재심의 판정을 받으며, 시범사업의 취지와 어긋나고 있다는 지적이 나온 바 있다.
이에 심평원 김국희 약제관리실장은 "시범사업이 대상 약제의 급여를 전제하는 것은 아니다"며 "심사과정에서 필요에 따라 추가 검토 기간이 소요될 수 있다"고 설명했다.
같은 시범사업 1호 약제로 지난해 말 급여 등재된 레코르다티의 콰지바(디누툭시맙베타)에 이어 빌베이도 재심에서 약평위를 통과해 시범사업의 성과가 입증된 셈이다.
한편, 이날 약평위에서는 HLB제약 씨트렐린구강붕해정 5mg(탈티렐린수화물)의 급여 적정성도 심의됐다. 신청 적응증은 '척수 소뇌 변성증에 의한 운동실조의 개선'이다. 약평위는 평가금액 이하 수용이라는 조건부로 급여 적정성을 인정했다.
관련기사
