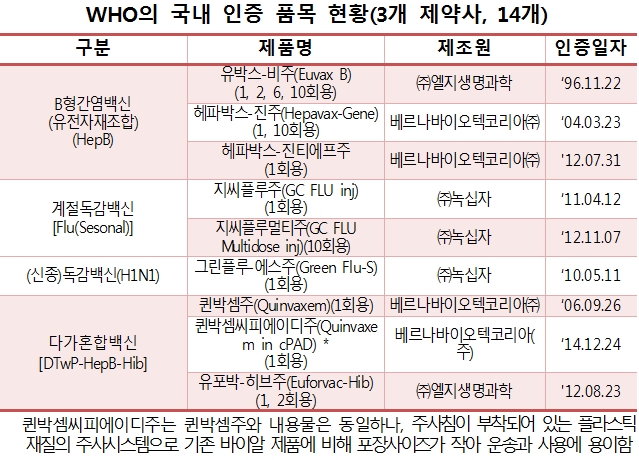
국산 백신 14개 WHO 사전 적격성평가 인증
식품의약품안전처(처장 정승)는 WHO 사전적격성평가(PQ)인증을 희망하는 국내 백신 제조사를 대상으로 'WHO PQ 인증지원을 위한 맞춤형 상담 및 현장자문'을 올해부터 확대 실시한다.
PQ는 WHO가 저개발국가 공급을 목적으로 백신 등의 품질 및 안전성·유효성 및 생산국 규제당국의 안전관리 역량을 포함해 평가하는 제도다. 이번 맞춤형 상담 및 현장자문은 WHO PQ 인증을 통해 국내 백신의 해외 인지도와 신뢰도 향상 뿐 아니라 국제 백신 조달시장에서 수출도 선점하는 것을 지원하기 위해 마련했다.
주요 지원 내용은 △임상·품질 등 PQ 신청 문서 작성법 △WHO 제조 및 품질관리 기준 실사 정보 및 사례 △백신바이알모니터(VVM) 표시라벨 제작·부착 요령 등 교육 등이다.
또 WHO PQ 인증에 필요한 실사에 대비해 현장 맞춤식 상담과 모의실사를 제공하고 신청에 필수적인 신청 문서의 내용 및 구성 등도 안내한다.
참고로 2013년 기준으로 국내 백신의 수출규모는 약 2억달러로 이중 WHO의 PQ 인증을 통한 수출이 95%(1억9000만 달러)에 해당하며 바이오의약품 전체 수출(4억 달러)과 비교하면 47%에 해당한다. 최초 인증품목은 '유박스-비주'(1996년)이고 지난해 말까지 백신 14개 폼목이 인증을 받았으며 WHO가 PQ 인증한 전체 백신 수, 230개 중 국내 품목은 6.1%를 차지하고 있다.
특히 지난해 12월 WHO는 '퀸박셈씨피에이디주'를 인증하면서 자체 실사를 생략하고 식약처의 실사 결과를 공유해 8개월 만에 인증한 바 있다.
식약처 관계자는 "이번 맞춤형 상담 및 현장자문을 통해 국내 제약사의 WHO PQ 인증 기간을 단축하고 글로벌 시장을 선점하는데 도움이 될 것"이라고 기대했다.