가톨릭의대 김동하 교수, 'C/EBPγ' 조절인자 기능 세계 최초 검증
당뇨병·암·신경성 퇴행성질환 등 질환 치료제 개발 기대

[메디칼업저버 박선혜 기자] 국내 연구팀이 당뇨병, 암, 신경성 퇴행성질환 등을 치료하는 과정에서 세포 항상성을 유지하기 위해 필요한 '오토파지(Autophagy)' 시스템을 조절하는 새로운 인자를 발견했다.
가톨릭의대 해부학교실 김동하 교수팀은 단일세포 유전체분석법을 활용해 오토파지의 새로운 조절인자인 'C/EBPγ' 기능을 세계 최초로 검증했다.
오토파지를 조절하는 과정과 조절인자를 새롭게 발굴하는 것이 관련 질환을 극복하는 데 매우 중요한 과제였던 점에서, 이번 연구 결과는 오토파지 기능 문제로 생길 수 있는 다양한 질환의 치료 후보물질 개발 가능성을 높일 것으로 기대된다.
오토파지는 세포 항상성을 유지하기 위해 불필요한 단백질이나 손상된 세포소기관을 제거하는 세포 내 분해 및 재활용 시스템이다. 세포 항상성을 유지하는 과정에서 오토파지를 일으키는 데 필요한 오토파지 단백질들도 불가피하게 분해된다.
이 때문에 일정한 수준의 오토파지가 유지되기 위해서는 해당 유전자가 활성화돼 오토파지 단백질을 만들고 세포 내에서 단백질량이 충분히 유지돼야 한다. 하지만 시스템에 문제가 생기면 당뇨병, 암, 신경성 퇴행성질환 등 질환이 유발된다.
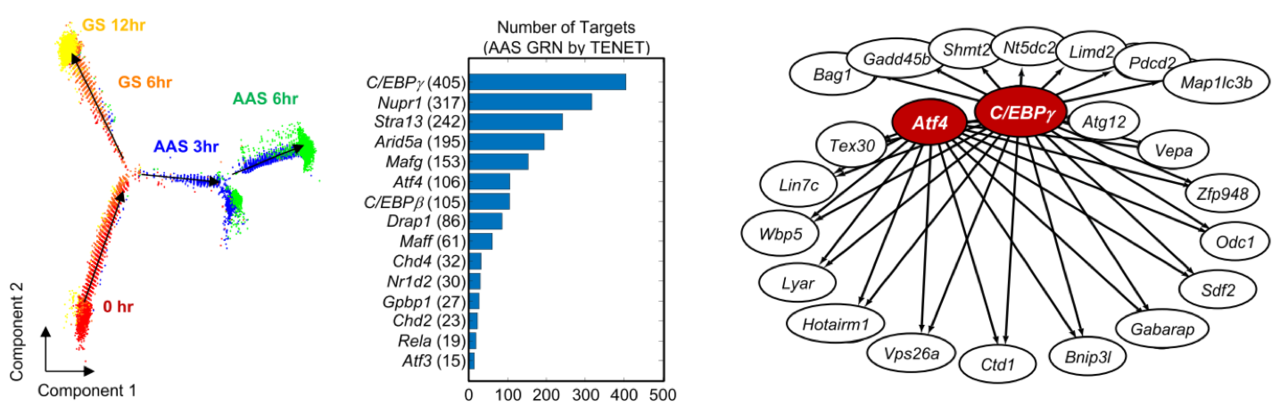
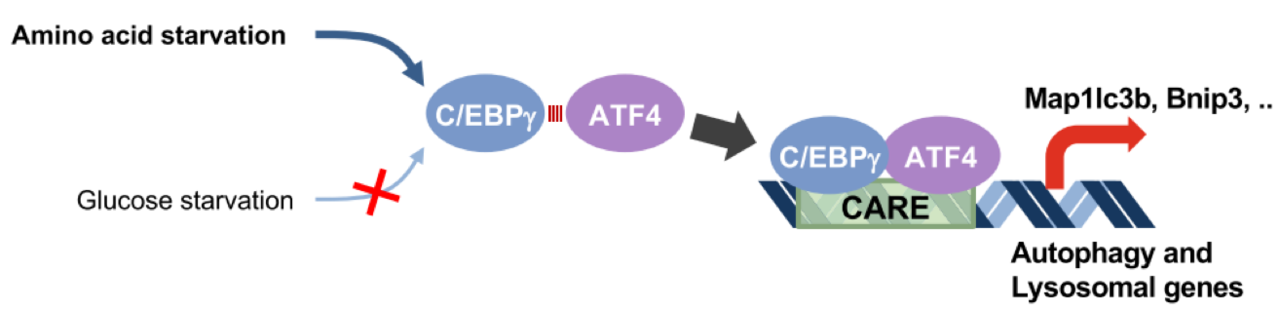
이번 연구에서는 C/EBPγ가 기존에 알려지지 않은 영양소 결핍 유형에 따라 특이적으로 작동하는 오토파지 조절인자로, 오토파지 유도의 다양한 신호 중 아미노산 결핍에 특이적으로 반응해 관련 유전자들을 활성화시킨다는 것을 밝혀냈다.
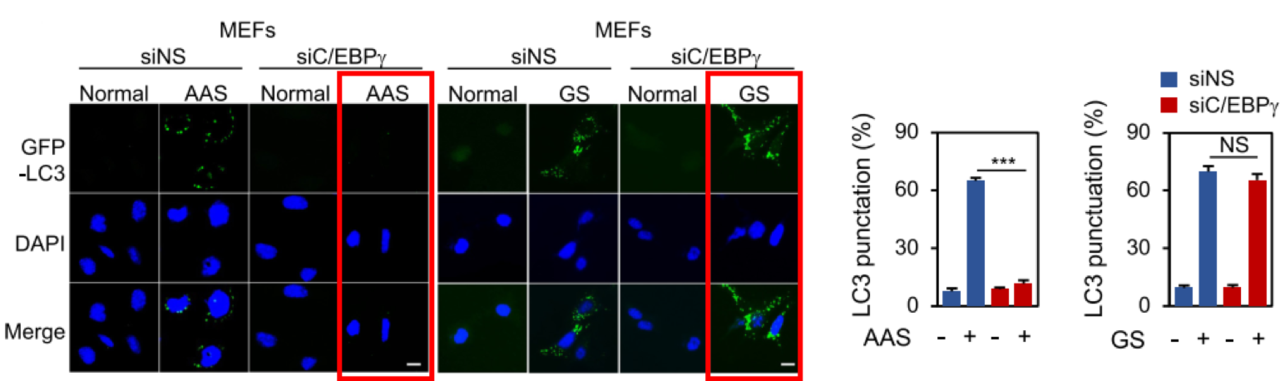
특히 연구에서 규명된 아미노산 결핍에 특이적으로 작용하는 C/EBPγ 기전을 이용한 오토파지 조절제는 오토파지 기능 문제로 인해 발생하는 다양한 대사질환, 퇴행성 뇌질환, 암, 심혈관질환 등 치료제 개발 시 아미노산 조절을 표적해 유용하게 사용될 것으로 전망된다.
김동하 교수는 "단일세포유전체 분석법으로 새로운 오토파지 조절인자를 예측하고 검증하는 연구를 처음으로 성공적으로 마무리하게 돼 놀랍고 기쁘다"며 "앞으로 다양한 질환 연구에서 이러한 접근법을 반영해 질병을 유발하는 새로운 인자를 더 빠르고 정확하게 검증해 난치성 질환 치료제를 개발하는 기반을 마련하고 싶다"고 밝혔다.
한편 이번 연구 결과는 Nucleic Acids Research 최근호에 실렸다.

