최근 '다발성경화증 치료의 최신 지견'을 주제로 심포지엄이 개최됐다.
좌장은 울산의대 김광국 교수와 국립암센터 김호진 교수가 맡았으며, 성균관의대 민주홍 교수, 국립암센터 김수현 교수가 차례로 강연했다.
본지에서는 이날의 강연을 요약·정리했다.

울산의대 교수
서울아산병원 신경과

국립암센터 교수
지원진료센터 신경클리닉
다발성경화증의 치료 최적화 전략

다발성경화증의 효과적인 치료를 위해서는 1) 효능, 2) 안전성, 3) 복약순응도 등을 고려한 치료 최적화 전략이 필요하다. 현재 국내 다발성경화증 치료법은 단계적 확대 전략의 관점에서 1차 치료제로 초치료 후에 효과가 없다고 판단되면 2차 치료제로 확대 전환할 수 있다.
Peginterferon beta-1a
다발성경화증 환자에서 낮은 복약순응도는 재발 위험을 증가시키는 것으로 알려져 있으며, 주사 제제의 투여 횟수가 빈번할수록 복약순응도는 감소한다. Peginterferon beta-1a는 pegylation된 약물로 기존 interferon 제제에 비해 화학적 안정성, 용해도, 안전성 및 내약성이 우수하다.
▶효능 평가
ADVANCE year 1 연구에서 1,516명의 환자를 위약, peginterferon beta-1a Q4W 및 peginterferon beta-1a Q2W (현 사용 용법) 투여군으로 무작위 배정해 1년 추적 관찰한 결과, Q2W 투여군에서 위약 대비 연간 재발률이 36% 감소, 재발 환자 위험도 39% 감소, 12주 장애 진행도 38% 감소 및 24주 장애 진행도 54%의 감소를 확인했다.
MRI 상에서 신생/신생 확대 T2 병변 수는 위약군 대비 67% 감소, 총 T2 병변의 용적에서도 유의한 감소가 관찰됐으며, Gd-증진(Gd+) 병변 또한 6개월 째 81%, 1년 째 86% 감소했다.
질병 무활성 근거(no evidence of disease activity, NEDA)에 도달한 환자의 비율은 Q2W 투여군에서 MRI 결과 기준 64%, 임상적 지표 기준 79%, MRI 및 임상 증상 모두 고려 시 54%로 위약 대비 유의하게 높았다.
ADVANCE year 2 연구에서는 ADVANCE year 1에서와 동일 피험자군에 대해 기존 peginterferon beta-1a 투여군은 치료를 지속하고 기존 위약 대조군은 peginterferon beta-1a Q4W 투여 또는 Q2W 투여하는 치료 지연군으로 전환해 효능을 비교했다.
그 결과 기존 Q2W 투여군은 치료 지연군 대비 37%의 연간 재발률 감소, 39%의 재발 환자 비율 감소를 보였고, 장애 진행도 역시 기존 12주에서 33%, 24주에서 41% 감소해 더 효과적인 것으로 나타났다.
MRI 결과에서도 T1 hypointense 병변 58%, 신생 활성 Gd+ 병변 65%, 신생/신생 확대 T2 병변 66% 감소해 모두 기존 Q2W 투여군이 치료 지연군보다 유의하게 감소했다.
▶안전성 평가
Peginterferon beta-1a 투여 시 항체 생성량을 측정한 결과, 결합 항체, 중화 항체, anti-PEG 항체는 각각 6%, 1% 미만, 7%로 peginterferon beta-1a Q4W 및 Q2W 투여군 모두에서 낮은 수준이었다. 또한, 임상적 상태와는 무관하며, 안전하다고 보고됐다.
전반적 위험성 평가 결과에서 대부분의 효능 관련 요인은 peginterferon beta-1a 투여군이 상대적으로 더 유익했으며, 감기 유사 증상, 간 수치 상승 및 백혈구 수치 감소 정도는 위약에서 더 유익했다.
Peginterferon beta-1a Q2W 투여 후 안전성 측면에 대해 추적 관찰한 결과, 투여 2년 후 및 3~6년 후에 감기 유사 증상 및 주사 부위 반응(injection site reaction, ISR) 발생 비율이 크게 증가하지 않는 것으로 보아 peginterferon beta-1a 투여가 장기적으로도 안전할 것으로 보인다.
Dimethyl fumarate
▶효능 및 안전성 평가
DEFINE 연구에서 1,237명의 환자를 위약 대조군, dimethyl fumarate BID 투여군(현 사용 용법) 및 dimethyl fumarate TID 투여군의 3개 군으로 1:1:1 무작위 배정한 뒤 2년간 추적 조사했다.
그 결과 BID 투여군에서 위약 대비 재발 환자 비율은 49% 감소, 2년째 연간 재발률은 53% 감소했으며, 12주 장애 진행도는 위약 대비 BID 투여군에서 38% 감소했다. MRI 상의 평균 병변 수를 비교했을 때 신생/신생 확대 T2 병변, Gd+ 병변 및 신생 T1 병변에 대해서 BID 투여군이 위약 대비 각각 85%, 90%, 72%의 감소를 보였다<그림 1>.
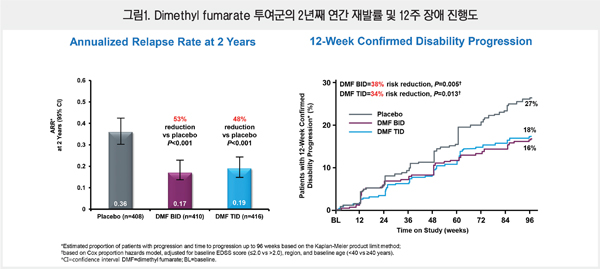
▶Glatiramer acetate와의 효능 비교 분석
CONFIRM 연구에서 1,430명의 환자를 위약 대조군, dimethyl fumarate BID 투여군, dimethyl fumarate TID 투여군, glatiramer acetate 투여군의 4개 군으로 1:1:1:1 무작위 배정한 뒤 투여 후 2년간 추적 관찰했다.
연간 재발률의 경우 dimethyl fumarate BID 투여군은 위약 대비 44% 감소(glatiramer acetate 투여군 29% 감소), 재발 환자의 비율은 34% 감소했다. 12주 장애 진행도 또한 dimethyl fumarate BID 투여군이 위약 대비 21% 감소해 glatiramer acetate 투여군의 7% 감소에 비해 효과적이었다.
Dimethyl fumarate BID 투여군과 glatiramer acetate 투여군에서 MRI 상 평균 병변 수의 위약 대비 감소 정도를 비교해보면 신생/신생 확대 T2 병변, 신생 T1 hypointense 병변, Gd2+ 병변 모두 dimethyl fumarate BID 투여가 glatiramer acetate 투여 대비 유의하게 감소했다.
CONFIRM 연구에서와 동일한 피험자군에서 기존 dimethyl fumarate 투여군은 똑같이 유지하되 기존 위약 또는 glatiramer acetate 투여군은 dimethyl fumarate BID 또는 TID 투여군으로 1:1 무작위 전환해 5년간 연장 추적 관찰한 ENDORSE 연구가 진행됐다.
연간 재발률이 기존 dimethyl fumarate 투여군에서 낮은 수준으로 유지되며, 기존 위약/glatiramer acetate 투여군은 dimethyl fumarate로 전환 후 감소하는 경향을 보였다.
재발 환자의 비율도 5년째 기존 dimethyl fumarate BID 투여군은 40%, 위약 투여 후 dimethyl fumarate 전환군은 53%였다. 24주 장애 진행도 및 MRI 상의 T2 병변, T1 병변, Gd+ 병변 모두 dimethyl fumarate로의 전환이 유의한 개선을 유도했다.
다발성경화증 치료제로서 natalizumab의 역할

국립암센터 교수
지원진료센터 신경클리닉
효능 분석 및 다른 약제와의 효능 비교
AFFIRM 연구에 따르면 942명의 환자를 natalizumab 투여군, 위약 대조군에 각각 2:1의 비율로 무작위 배정한 뒤 2년간 추적 관찰한 결과, 연간 재발률이 natalizumab 투여군에서 위약 대비 68% 감소, 고활동성 환자군에서는 81%(p<0.001)의 감소를 보였다. 24주 장애 진행도 또한 투여군에서 위약 대비 64%(HR 0.36, p=0.004) 감소했다.
4,332명의 환자를 대상으로 성향 점수(propensity score)를 이용한 연구에서 연간 재발률 측면에서 alemtuzumab이 IFN-beta 및 fingolimod에 비해 더 유익했던 반면, natalizumab과는 유사했다. 장애 누적도의 경우 alemtuzumab과 natalizumab간에 차이가 유의하지 않았으나 장애 개선도에서는 natalizumab이 alemtuzumab보다 더 효과적이었다(HR 0.35, 95% CI 0.20~0.59, p=0.0006).
PML 발생 위험에 대한 이해
Natalizumab의 선택에 있어 가장 우려되는 점은 진행성 다초점성 백질뇌병증(progressive multifocal leukoencephalopathy, PML)의 발생 위험이다. 그러나 위험성과 그 정도에 대해 정확히 이해하고 예방한다면 현명하게 natalizumab을 사용할 수 있다.
2017년 9월 기준 전세계 natalizumab 사용 환자 수는 17만 4,400명에 달하며, 1,000명당 약 4명의 PML 발생률을 나타낸다. 현재까지 749명의 PML 사례가 있었고 이중 76%는 장애 정도는 다양하지만 생존하고 있다. PML의 평균 발생 시점은 natalizumab 투여 후 약 49개월이었다.
Anti-JCV 항체 검사
JC 바이러스에 대한 노출 여부는 PML 발생 예측의 중요한 지표이며, anti-JCV 항체 검사를 통해 노출 여부를 파악할 수 있다. Natalizumab 치료를 고려하면 반드시 치료 전 anti-JCV 검사를 시행해야 하며, 치료 전 음성인 환자에서는 6개월 간격으로 추적 검사를 권고한다.
Natalizuamb 치료 중 anti-JCV seronconvertion (음성→양성)은 매해 3~ 8% 정도로 보고되고 있다. 치료 전후 anti-JCV 항체 검사에서 단 한 번이라도 양성 판정을 받은 환자는 양성으로 간주해 모니터링해야 한다.
Anti-JCV 항체의 양성 비율은 서구권의 경우 평균적으로 다발성경화증 환자의 55% 정도로 보고되고 있는 반면, 국내 환자의 경우 87%에 달한다(국립암센터 내 31명의 환자 검사 결과). 일본에서도 치료 시작 전 환자의 70%에서 anti-JCV 항체 양성이 보고된 바 동양에서 보다 높은 anti-JCV 항체의 seroprevalence의 경향이 의심되며, 따라서 현재의 PML 감시 가이드라인을 국내 환자에 적용할 때 향후 연구가 더 필요할 것으로 보인다.
PML의 주요 위험 요인 및 감시 가이드라인
PML의 세 가지 주요 위험 요인은 1) anti-JCV 항체 양성 여부 및 index 값, 2) natalizumab 치료 2년 이상, 3) 치료 전 면역억제제 사용력이다.
Anti-JCV 항체가 음성인 경우 PML의 발생 위험은 극히 낮으며, 양성인 경우에는 index 값이 높을수록 위험도가 증가하는 것으로 나타나지만 natalizumab 사용 2년 이전까지는 index 1.5 이상에서도 발생 위험이 0.9%로 낮은 편이다.
면역억제제 사용력이 있는 경우에는 index 값에 의한 영향이 없으나 치료 기간이 길어질수록 위험도가 증가하는 경향은 같다. 세 가지 주요 위험 요인을 동시에 고려할 때 PML 예방을 위한 감시 가이드라인은 다음과 같다<그림2>.
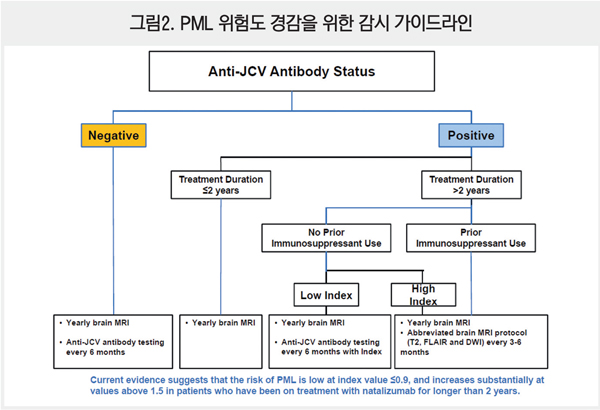
PML의 임상적 특징
PML의 임상적 특징이 다발성경화증과 유사해 적절한 감별이 필요하다. Natalizumab 치료는 기본적으로 높은 NEDA 달성률을 보이기 때문에 환자에게 새로운 신경학적 증상이 발생했을 시에는 일단 PML을 의심해봐야 한다.
대개 다발성경화증은 급성인 반면에 PML은 비교적 아급성으로 점진적으로 진행되며, 인지적 변화, 뇌전증 및 운동장애 등을 동반한다. MRI 상에서 PML 병변은 3 cm 이상으로 큰 편이며, 회질에 subcortical U-fiber의 침범, 두드러진 FLAIR 병변, diffusion에서의 high intensity 등의 특징을 갖는다.
차후 대체 약제로의 전환 전략
Natalizumab의 장기간 사용은 PML의 발생 위험 증가를 수반하기 때문에 다른 약제로의 적절한 전환이 중요하며, 전환 시 다음의 세 가지 측면에서 고려해야 한다.
▶질병 활성도의 반동(rebound) 현상
Natalizumab 중단 시 질병의 재발이 2~6개월 뒤부터 나타나기 시작하고, 5~8개월에 최고점에 도달하게 된다. 중단 이후 연간 재발률은 상승하나 치료 전 수준을 초과하지 않으며, 이후 다른 치료제를 통해 ~90%의 환자에서 확장형장애척도점수가 안정적으로 유지되는 것으로 보고된다.
▶중단 후 고려 가능한 약제
Natalizumab 중단 후 대체 약제로서 fingolimod가 다른 interferon 주사 제제와 비교했을 때 재발률 측면에서 질병 조절에 더 효과적이었으며, 스웨덴에서는 natalizumab을 rituximab으로 대체해 fingolimod으로의 대체에 비해 재발률, 부작용 및 복약순응도 측면에서 더 우월함을 확인한 사례도 있다.
▶휴약기
Natalizumab은 CNS 내로의 림프구 유입을 억제하므로 면역감시의 보존을 위해서 약제 전환 시 휴약기가 필요하다. 안전성 측면에서 natalizumab의 마지막 투여 후 주로 8~12주 사이에 새로운 약을 시작할 것을 권고한다.
Q&A
Q: Alemtuzumab를 사용하다 재발하는 환자에 있어서 그 대안으로 natalizumab을 사용할 수 있습니까?
A: Alemtuzumab 치료가 실패한 환자에서 사용 가능한 대체 약물에 대한 증거가 아직 불충분합니다. Alemtuzumab과 같이 강력한 면역억제제를 사용한 후에 natalizumab을 먼저 고려하는 것은 기회 감염의 위험성이 염려되지만 강력한 조절이 필요한 상황에서는 1년 전후의 natalizumab 사용을 고려해볼 수 있을 것입니다.
Q: JCV 항체 검사 시 유니랩에 보내는 것과 국내에서 하는 것의 차이점은 무엇입니까?
A: 유니랩에서 하는 검사는 JCV 항체를 감지해 측정하는 것이며, 국내에는 항체를 측정할 수 있는 실험실이 없어 JCV DNA를 PCR해 감지하는 것으로 대신하므로 민감도가 굉장히 낮아 고감도의 PCR 장비가 필요한데 국내에는 이런 장비가 없기 때문에 국내 검사는 무의미하다고 볼 수 있습니다.
정리·메디칼라이터부

