치아는 아름다운 미소와 美뿐만 아니라 음식물 섭취 기능부터 사회적 활동 및 전반적인 삶의 질과 건강에도 큰 영향을 미친다1. 따라서 꾸준하고 장기적인 치아 관리는 행복한 일상을 위해 필수적이다2,3.
그러나 이러한 치아 건강을 방해하는 흔한 증상 중 하나는 ‘시린이’이다. 시린이 또는 상아질 지각과민증(dentin hypersensitivity)은 만성적인 증상으로 나타나며, 노출된 상아질이 여러 자극에 반응하여 짧고 날카로운 통증으로 나타나는 것을 의미한다<그림 1>2,4,5.
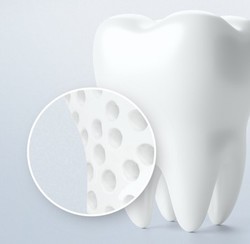
실제로 약 3명 중 1명이 지각과민증을 경험하고 있으며6, 2021년 건강보험심사평가원 자료에 따르면 지각과민증 처치를 받은 국내 환자는 최근 10년간 꾸준히 증가한 것으로 보고되었다2. 지각과민증의 주된 위험 요인은 잘못된 칫솔질7, 치과 치료2, 그리고 음식으로 인한 구강 산성 환경8 등이 있다. 자연적으로 시간이 지남에 따라 노출된 상아세관이 부분적으로 밀폐하여 불편함 및 증상이 감소하기도 하지만, 이러한 자연적 밀폐는 산성 환경에 취약하며 많은 환자가 계속해서 통증을 겪고 있으므로 이를 해결하는 것은 임상가들의 중요한 숙제이다2,8,9.
지각과민증 치료는 장기적인 관리가 중요하며, 원인 제거 및 불소 제재나 지각과민증을 위한 전용 치약 등을 이용한 홈 케어부터 시작한다2,5. 현재 다양한 시린이 치약이 출시되어 있으며, 기전은 주로 다음과 같이 두 가지로 나뉜다: 1) 신경 둔감화(nerve desensitization), 및 2) 상아세관 밀폐(occlusion of dentinal tubules)5. 상아세관을 부분적으로 밀폐하는 시린이 치약으로 센소다인의 1세대 치약인 오리지널이 대표적이다5. 시린이 치약 2세대로 개발된 센소다인의 멀티케어는 신경 둔감 기전을 이용해 시린이(지각과민증) 증상을 완화한다2,10. 2023년 8월에 출시된 센소다인의 3세대 시린이 치약 리페어&프로텍트는 상아세관을 밀폐할 뿐만 아니라 표면과 내부에 보호층을 형성하여 시린이(지각과민증) 증상을 완화 및 예방한다8,11,12.
과립의 형태로 상아세관을 일부 밀폐하는 염화스트론튬 포함 1세대 시린이 치약,
센소다인 오리지널
염화스트론튬(strontium chloride)은 약 50년 전에 처음으로 상아세관 밀폐 기전의 치약에 첨가된 생리활성 물질이며, 센소다인의 1세대 시린이 치약인 오리지널의 주요 유효 성분이다13. 염화스트론튬은 노출된 상아세관을 물리적으로 막아 지각과민증 증상을 완화해준다2,5. 구체적으로, 스트론튬(strontium) 성분의 치약을 사용 시, 스트론튬 성분이 상아세관 내에 침투하여 과립의 형태로 상아세관을 부분적으로 밀폐한다 <그림 2>14,15.
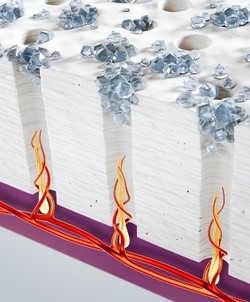
이로 인해 상아세관액의 이동을 방지하여 말초신경 자극을 줄여주는 것으로 알려져 있다5,13. 국내에서 진행된 시험관 내(in vitro)연구에서는 일부 시린이 치약들의 상아세관 폐쇄 효과를 평가하였다4. 분당 50회의 칫솔질을 상아세관이 개방된 시편에 시행한 후 주사전자현미경(SEM)을 이용하여 상아세관의 크기 변화를 관찰하였고, 그 결과 염화스트론튬의 유효성분이 함유된 치약으로 처치한 경우, 상아세관이 일부 폐쇄되거나 면적이 줄어들었다4. 이에 따라, 개방된 상아세관의 수 또한 감소하였다4. 이와 같은 염화스트론튬 기전을 통한 통증 완화 효과는 임상연구에서도 입증되었다16. 치과 치료 후 지각과민증 증상이 있는 환자들에게 염화스트론튬이 함유된 치약을 7주 동안 사용한 결과, 기저 시점 대비 통증이 약 76% (p <0.01) 감소하였으며, 이는 약 34%로 감소된 placebo 군에 비해 약 두 배 이상 개선된 수치다16.
질산칼륨 포함한 2세대 시린이 치약 센소다인 멀티케어, 신경을 둔감시켜 시린이 예방 및 완화
질산칼륨(potassium nitrate)을 함유한 시린이 치약은 1980년 이후부터 현재까지 사용되어온 신경 탈감작 기전의 치약이며17, 센소다인의 2세대 치약인 멀티케어의 주요 성분이다10. 칼륨(K+)은 노출된 상아세관 사이로 흡수되어 상아세관 기저부에 있는 신경을 향해 이동하며<그림 3>, 상아질 표면 주변에 칼륨 농도를 증가시킨다2,17.
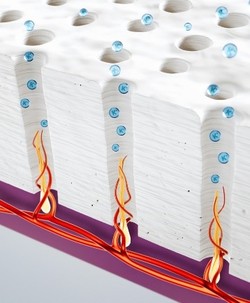
세포 외 높은 칼륨 농도는 전위차로 인한 전기적 자극을 감소시켜 치아 내 신경(intradental nerve)의 활성을 저하시키는데, 이러한 신경 활성 감소로 지각과민증을 예방 및 완화시켜준다<그림 4>5,17-19.

질산칼륨 기반 치약은 임상시험을 통해 민감성 감소 효과를 입증했다20. 하루에 2번 질산칼륨 기반 치약(n=18)을 사용한 후 2, 4, 8, 12주째 민감성 증상을 평가한 결과, 대조군(n=18) 대비 실험군은 4주째부터 tactile 및 cold air에 대한 자극 감소 및 통증 완화 효과를 보였다20. 12주째에 질산칼륨 기반 치약 사용자는 tactile 및 cold air에 대한 자극이 기저 시점 대비 약 80% 감소했다고 보고했으며(vs. 22-27% 대조군; p <0.01), 67%가 주관적인 통증이 거의 사라졌다고 보고했다(vs. 6% 대조군; p <0.01)20. 이러한 결과로 보아, 질산칼륨 기반 치약을 하루에 2번 이상 사용할 시 4주부터 증상 개선 효과를 볼 수 있으므로, 지각과민증 예방과 증상 완화 효과를 위해 꾸준하고 장기적인 사용이 필요하다20.
표면과 내부 보호층 형성을 통해 상아세관을 밀폐하는 플루오르화석이 포함된 3세대 시린이 치약 센소다인 리페어&프로텍트
센소다인 1세대 시린이 치약을 비롯한 여러 시린이 치약이 다양한 상아세관 밀폐 기전을 통해 약 몇 십년 동안 지각과민증 완화를 위해 사용됐다5,21. 그 중에서도 플루오르화석(stannous fluoride) 성분을 함유한 센소다인의 3세대 시린이 치약 리페어&프로텍트는 최근 2023년 8월 새로운 작용기전을 도입하여 출시되었다12. 플루오르화석 성분은 물이나 일반적으로 타액에서 발견되는 특정 음이온이 있을 때 빠르게 산화 및 가수분해되어 미세한 상아세관 틈새에 깊숙이 침투한다14,22,23. 이렇게 침투된 성분들은 상아질 표면 및 상아세관 내에 침전되는 불용성 금속 화합물을 형성하여 상아세관을 폐쇄하고<그림 5> 보호층을 생성한다<그림 6>5,11,14,21.


보호층 생성 과정을 더 자세히 설명하자면, 구강 내 pH가 내려가 산성 환경이 조성될 때, 상아질의 수산화아파타이트(hydroxyapatite)가 일시적으로 탈회하여 pH 균형을 잡는다22. 이 때 플루오르화석의 성분인 플루오르화물(fluoride)이 있는 경우, 플루오라파타이트(fluorapatite)가 형성되어 탈회된 상아질에 결합하여 재광화를 촉진한다5,22. 이러한 재광화는 보호층을 형성하고 상아질을 더 단단하게 만들어 추가적인 탈회 및 자극에서부터 보호하고 궁극적으로 상아질 투과성을 감소시켜 지각과민증을 예방하고 완화한다5,14,22,24. 한 임상연구에 따르면, 플루오르화석 기반 치약을 8주간 사용한 결과, 기저 시점 대비 지각과민증 증상(Schiff) 점수가 약 66% 개선되었으며, 불소만 함유한 치약 대비 약 63% 더 효과적이었다(p <0.0001)24. 또한, 한 메타분석에 따르면, 플루오르화석은 다른 플루오르화합물(i.e., amine fluoride, sodium monofluorophosphate, or sodium fluoride)보다 tactile과 air 자극에 더 좋은 효과를 보였다(각각 SMD 2.02, 95% CI 1.06-2.99; SMD 1.9, 95% CI 1.03-2.77)25.
플루오르화석의 상아세관 폐쇄 효과와 보호층의 효과는 과학적으로 입증됐다8,26. 한 연구에서 하루 2회 4일간 플루오르화석 기반 치약을 사용한 후 SEM을 통해 상아질을 관찰한 결과, 노출된 상아세관이 대부분 폐쇄되었다26. 한 시험관 내 연구에서, 일반 충치 예방 치약(대조군)과 불화주석 기반의 치약의 산 보호 효과에 대해 비교해 보았다8. 각 치약을 시편으로 제작된 상아질 원판에 도포하고 산성환경을 조성하는 탄산음료에 약 10분간 넣어 SEM과 주사현미경(CLSM)을 통해 상아질 표면의 변화를 관찰하였다8. 그 결과, 대조군의 상아질 도말층(smear layer)은 2분 만에 용해되었으며, 10분 후 대부분의 상아세관이 노출되어 있었다8. 반면, 플루오르화석 기반의 치약을 도포한 상아질의 도말층 침식은 관찰되지 않았으며, 노출된 상아세관이 거의 없었다8. 이러한 결과는 플루오르화석 기반 치약이 산성 환경에서 상아질을 효과적으로 보호하여 지각과민증 증상을 예방하고 완화하는 것을 시사한다8,24.
지각과민증은 장기간 반복적으로 나타나는 증상이기 때문에 삶의 질을 개선하기 위해 매일 장기간 플루오르화석과 같은 시린이 치약을 사용하는 것이 중요하다27,28. 한 연구에서 플루오르화석 기반 치약을 매일 2회 24주간 지각과민증이 있는 환자가 사용했을 시 삶의 질이 8주부터 기저 시점 대비 지속적으로 개선되었다(p <0.0001)28. 이는 시린이 치약을 꾸준하게 장기간 사용할 시 삶의 질에 긍정적인 영향을 미칠 수 있는 것을 보여준다28.
고찰
센소다인의 시린이 치약은 시간이 지남에 따라 3세대를 거듭하여 개발되었다10,12,13. 처음 개발된 1세대 시린이 치약 오리지널은 염화스트론튬을 통해 상아세관을 부분적으로 밀폐하여 통증을 완화시켰으며4,14,16, 그 뒤 질산칼륨을 함유한 2세대 시린이 치약 멀티케어는 신경 둔감화를 이용해 시린이(지각과민증) 예방 및 증상을 개선시켰다2,10,20. 그리고 최근 국내에 출시된 3세대 시린이 치약 리페어&프로텍트의 플루오르화석 성분은 상아세관 깊숙이 침투하여 보호층을 형성하는 작용기전을 가지고 있다5,12,14. 플루오르화석 기반 치약은 증상 완화 및 예방뿐만 아니라 매일 장기간 사용으로 삶의 질도 향상시킬 수 있다28. 이러한 여러 세대의 시린이 치약은 임상가들을 위한 치료 전략에 다양한 치료 옵션을 제공한다.
CI, confidence interval; CLSM, confocal laser scanning microscopy; SEM, scanning electron microscope; SMD, standardized mean difference
References
1. Tadin A, et al. Healthcare (Basel) 2022;10(2):406.
2. 전미정, 서덕규. 대한치과의사협회지 2022;60(4):216-223.
3. Lee B, Kim S. J Korean Acad Oral Health 2020;44(2):109-116.
4. Lee SY. J Dent Hyg Sci 2011;11(5):431-436.
5. 장지현. 대한치과의사협회지 2022;60(4):224-230.
6. Zeola LF, Soares PV, Cunha-Cruz J. J Dent 2019:81:1-6.
7. Davari AR, Ataei E, Assarzadeh H. J Dent Shiraz Univ Med Sci 2013;14(3):136-145.
8. Burnett G. Am J Dent 2013;26(Spec No A):15A-18A.
9. Jacobsen PL, Bruce G. J Contemp Dent Pract 2001;2(1):1-12.
10. 센소다인 멀티케어 허가사항
11. Miglani S, Aggarwal V, Ahuja B. J Conserv Dent 2010;13(4):218-224.
12. 센소다인 리페어&프로텍트 허가사항
13. de Melo Alencar C, et al. Open Dent J 2017;11:476-484.
14. Collaert B, Fischer C. Endod Dent Traumatol 1991;7(4):145-152.
15. Saeki K, et al. Dent Mater 2016;32(2):240-251.
16. Uchida A, et al. J Periodontol 1980;51(10):578-581.
17. Orchardson R. Strategy for the management of dentinal hypersensitivity. In: Addy M et al. (eds). 2000. Tooth Wear and Sensitivity. London: Martin Dunitz, pp. 315–325.
18. Stead WJ, Orchardson R, Warren PB. Arch Oral Biol 1996;41(7):679-687.
19. Peacock JM, Orchardson R. J Dent Res 1995;74(2):634-641.
20. Nagata T, et al. J Clin Periodontol 1994;21:217–221.
21. Hines D, et al. J Am Dent Assoc 2019;150(4S):S47-S59.
22. Fiorillo L, et al. Biomimetics (Basel) 2020;5(3):41.
23. Baig AA, et al. Int Dent J 2014;64(Suppl 1):4-10.
24. Parkinson CR, et al. Am J Dent 2015;28:181–244.
25. Martins CC, et al. J Dent Res 2020;99(5):514-522.
26. Takamizawa T, et al. J Oral Sci 2019;61(2):276-283.
27. Idon PI, et al. Front Dent 2019;16(5):325–334.
28. Mason S, et al. BMC Oral Health 2019;19:226.

