6세 이상 1형 당뇨병 환자 대상으로 iLet Bionic Pancreas 허가
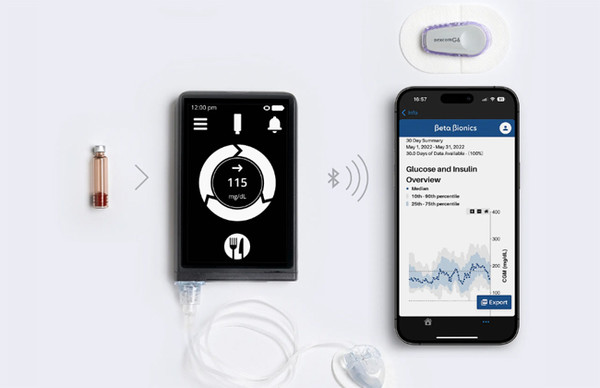
[메디칼업저버 박선재 기자] 미국 식품의약국(FDA)이 베타 바이오닉스(Beta Bionics)사가 개발한 전자동 인공 췌장 'iLet Bionic Pancreas'를 승인했다.
iLet Bionic Pancreas는 6세 이상 1형 당뇨병을 적응증으로 승인된 연속혈당측정기(CGM)와 함께 구동되는 소프트웨어다.
주머니에 들어가는 크기의 이 시스템에는 베타 바이오닉스 아이렛 에이스 펌프(Beta Bionics iLet ACE pump)와 아이렛(iLet) 투약 결정 소프트웨어가 장착돼 있다.
지금까지의 인공췌장(closed-loop system, 폐루프기기)은 환자가 인슐린 양과 시간 등을 입력해야 했다. 그런데 이번에 승인된 iLet Bionic Pancreas는 처음에만 체중을 입력하면 기기를가 혈당 정보를 학습해 환자에게 맞는 인슐린 양이 자동으로 투여된다.
iLet Bionic Pancreas의 유효성 데이터는 지난해 9월 NEJM에 발표된 바 있다.
그 내용을 살펴보면, 13주 동안 표준치료군과 비교군을 비교한 연구에서 평균 당화혈색소(A1C)를 7.9%에서 7.3%로 낮췄다(CI -0.6~-0.3, P<0.001).
또 평균 목표혈당범위(70~180mg/dL) 내에 포함되는 시간도 표준치료군 11% 길어졌는데, 이는 하루에 2.6시간에 해당하는 수치다.
이외에도 고혈당(180mg/dL 이상)과 중증 고혈당(250mg/dL 이상)에 머무르는 시간도 현저하게 감소했다. 표준치료군에는 덱스콤 등 리얼 타임 CGM 등이 포함됐다.
FDA 기기 및 방사선 보건센터 Jeff Shuren 책임자는 "이번 FDA 승인은 1형 당뇨병 커뮤니티에 당뇨병 관리를 위한 추가적 옵션과 유연성을 제공할 것"이라며 "AID(자동 인슐린 투여) 기술의 범위를 넓히는 데 도움이 될 것"이라고 말했다.

