허가전담심사팀인 바이러스백터 백신팀에서 독성·약리·품질자료 검토
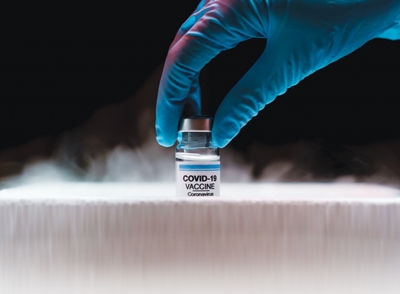
[메디칼업저버 정윤식 기자] 식품의약품안전처는 12월 22일 얀센社(존슨앤드존슨)가 코로나19(COVID-19) 백신 허가신청 전 사전검토를 신청했다고 밝혔습니다.
해당 백신은 정부에서 도입계획을 발표한 백신 중 하나로, 비임상·품질 자료에 대한 사전검토를 신청했다.
이에 허가전담심사팀인 '바이러스벡터 백신팀'에서 해당 백신의 독성, 약리, 품질자료를 사전에 면밀히 검토할 예정이다.
식약처는 코로나19 백신의 국내 허가신청을 대비해 신속심사를 위한 2개의 '허가전담심사팀'을 구성·운영 중이다(바이러스벡터 백신팀, 핵산 백신팀).
백신 개발업체는 품질, 비임상, 임상 등의 자료를 준비하는 대로 식약처에 제출해 허가신청 전 사전검토를 받을 수 있다.
식약처 관계자는 "이를 통해 백신의 안전성과 유효성을 충분히 검토할 수 있는 시간을 확보하고 허가신청 이후 심사에 걸리는 기간을 최대한 단축할 수 있을 것으로 기대한다"고 말했다.
관련기사
- 2025년까지 식·의약품 안전기술 최고국 수준 만든다
- 내년 보건산업 수출 256억 달러로 지속적 성장 전망
- 美 FDA 모더나 코로나19 백신 승인, 노바티스 인클리시란 거절
- 얀센·화이자 12월, 1월에 모더나 백신 계약 체결
- 방역당국 코로나19 백신 신속 접종 분위기 우려
- 政, 얀센·화이자와 코로나19 백신 계약 체결
- 질병청, 코로나19 백신 8600만회분 확보
- 코로나19 백신 AZ 1분기·얀센 2분기·화이자 3분기 도입
- 주요 12개국 코로나19 백신, 셋 중 하나는 아스트라제네카 제품
- [신년기획] 코로나19 백신 맞이하기 전에 준비할 것은?
- 모더나 코로나19 백신 2천만명분 공급하기로 합의
