이대약대 손경복 교수, 허가특허연계제도 도입 효과 분석
[메디칼업저버 이현주 기자] 허가특허연계제도(이하 허특제) 도입 이후 특허도전 시점은 빨라졌으나 신약의 유효독점 기간에는 영향을 미치지 못한 것으로 나타났다.
이화여대 약대 손경복 교수가 허특제 도입 효과를 분석하기 위해 허특제 도입이 신약 독점기간에 미친 영향을 사건분석(event history analysis)한 결과 이 같이 확인됐다.
손 교수는 지난 2007년부터 2011년까지 국내에서 허가받은 신약개수와 특허도전을 받은 품목, 그리고 특허도전 시점을 분석했다.
허가특허연계제도가 2015년 시행됐고, 신약의 시판 후 자료를 보호해 주는 기간인 재심사기간(PMS)이 6년인 것을 감안할 경우 2009년 이후 허가된 신약들은 해당 제도의 영향을 받은 것으로 볼 수 있다.
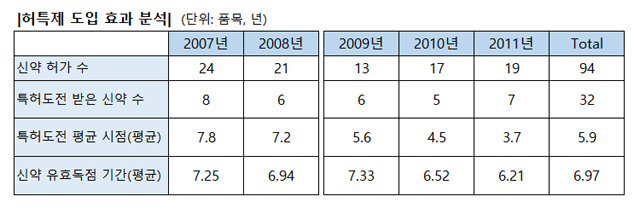
2007년과 2008년 허가받은 신약의 갯수는 각각 24개, 21개였으며 이들 중 8품목과 6품목이 특허도전을 받았다. 후발 의약품으로부터 특허 도전을 받은 시기는 2007년의 경우 허가 이후 평균 7.8년, 2008년은 7.2년이었다.
2009년에는 13개, 2010년 17개, 2011년 19개 신약이 허가됐으며 이들 중 특허 도전을 받은 신약은 각각 6개, 5개, 7개 품목이다. 특허도전까지 걸리는 시간은 2009년 평균 5.6년, 2010년 4.5년, 2011년 3.7년으로 분석됐다.
허특제 이전에는 보통 재심사기간이 만료된 이후 특허도전이 시작됐다면, 요즘은 재심사기간이 만료되기 2.3년 전부터 후발 의약품이 시장에 나올 채비를 서두르고 있었다.
그러나 신약의 유효 독점기간은 크게 변화하지 않은 것으로 나타났다.
실제 같은 기간을 기준으로 신약 독점이 유효했던 기간을 살펴보면 허특제가 영향을 미치지 않는 2007년은 평균 7.25년, 2008년 6.94년으로 나타났고, 이후인 2009년은 평균 7.33년, 2010년 6.52년, 2011년 6.21년이었다.
실제 수치 상으로는 신약이 독점할 수 있는 기간이 짧아진 것으로 보이나 통계적으로는 유의미하지 않다는 분석이다(P=0.1178).
손 교수는 "허특제가 미국과 캐나다, 호주 등 제한된 국가에서만 운영됐고, 제도의 효과를 실증적으로 분석한 연구가 없었다"며 "최근 한국에서 허특제 도입 효과를 실증적으로 분석한 것"이라고 설명했다.
식품의약품안전처는 이 같은 결과를 바탕으로 허특제 개선방안을 논의할 것으로 알려졌다.
