식약처, GBP510의 안전성 및 면역원성 임상시험 승인…재조합 백신 형태
지난해 12월말 기준 치료제 15개 제품, 백신 6개 제품 임상시험 진행 중

[메디칼업저버 정윤식 기자] 식품의약품안전처는 국내개발 코로나19(COVID-19) 백신 중 SK바이오사이언스의 'GBP510'의 임상시험을 지난해 31일 승인했다.
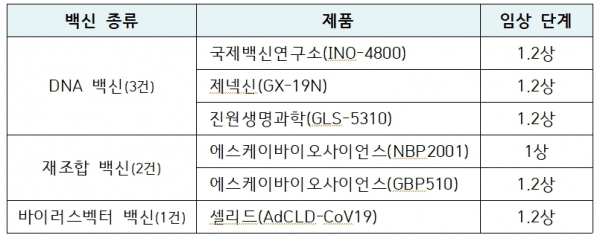
이에 현재 국내에서 코로나19와 관련해 임상시험을 승인받아 개발을 진행하고 있는 의약품은 치료제 15개 제품(13개 성분)과 백신 6개 제품이 됐다.
이번 임상시험은 건강한 성인을 대상으로 GBP510의 안전성 및 면역원성을 평가하기 위한 것으로 1상 진행 후 2상을 순차적으로 진행한다.
GBP510은 코로나19 바이러스의 '표면항원 단백질'을 유전자 재조합 기술을 이용해 만든 '재조합 백신'이다.
예방원리는 백신의 표면항원 단백질이 면역세포를 자극해 중화항체를 형성, 면역반응을 유도하며 코로나19 바이러스가 침입하는 경우 항체가 코로나19 바이러스를 제거하게 된다.
앞서 SK바이오사이언스가 지난해 11월 23일 임상(1상) 승인받은 재조합백신 'NBP2001'는 코로나19 바이러스의 표면 항원 단백질로 면역반응을 유도하는 반면에, 'GBP510'은 표면 항원 단백질이 나노구조(정20면체)를 형성하는 특정 단백질과 결합해 면역반응을 유도하는 차이가 있다.
해외에서도 미국의 노바백스가 유전자재조합 기술을 이용한 코로나19 백신의 임상시험(3상)을 진행하고 있는 것으로 알려졌다.
식약처 관계자는 "앞으로도 코로나19 치료제와 백신 개발에 대한 국민적 관심이 높은 점 등을 고려해 개발 제품의 임상시험 현황에 대한 정보를 신속하게 전달하겠다"고 말했다.
그는 이어 "안전하고 효과 있는 코로나19 치료제와 백신이 신속히 개발될 수 있도록 필요한 사항을 지원해 우리 국민이 치료 기회를 보장받을 수 있도록 최선을 다할 계획"이라고 덧붙였다.
- SK바이오사이언스- 서울대병원, 코로나 백신 임상시험 맞손
- 원희목 회장, "치료제와 백신 개발 성공하는 해 될 것"
- 셀트리온 CT-P59, 코로나 치료제 허가·심사 착수
- 코로나19 대유행...국회에서는 백신 확보 두고 여야 '공방전'
- 2021년 의약품 허가정책 주요 개선 내용 살펴보니
- 주요 12개국 코로나19 백신, 셋 중 하나는 아스트라제네카 제품
- 국민 절반 코로나19 백신 접종, 집단면역 생성 일상복귀 가능
- 4일부터 사회적 거리두기 2주간 연장
- SK바이오사이언스, GSK 백신 5종 공동판매 계약 체결
- 다국적사 백신 파트너 교체…기회와 위기 공존
- 방역당국, 노바백스 코로나19 백신 구매 논의 중
- SK바이오사이언스, 코로나 백신 임상3상 IND 제출
- 政, 2023년까지 mRNA 백신 1개 이상 국내개발키로
