불응성 환자 타깃 강점...SK바이오팜 "약효에서 차별"
UCB와 국내 시장 경쟁 예고...학계 "기존 치료제보단 낫지만..."

[메디칼업저버 양영구 기자] 20년 개발 끝에 미국식품의약국(FDA) 승인을 받은 SK바이오팜의 뇌전증 치료 신약 엑스코프리(성분명 세노바메이트).
엑스코프리는 SK바이오팜이 글로벌 임상 3상까지 진행해 FDA 허가를 받은 첫 신약인 만큼 시장성에 관심이 집중되고 있다.
우선 회사 측은 임상시험을 통해 입증한 약효와 안전성을 엑스코프리의 시장 경쟁력으로 꼽는다. 제약업계 역시 국내 시장을 장악하고 있는 UCB에 대적할 수 있는 상대로 보고 있다.
학계는 사뭇 다른 분위기다. 엑스코프리가 기존 뇌전증 치료제보다 좋은 임상 결과를 보인 건 맞지만, '획기적'이라고 칭하기에는 어렵다는 입장이다.
"엑스코프리, 차별성은 효과와 안전성"
대한뇌전증학회에 따르면 일반적으로 뇌전증 치료제를 처음 투여받은 환자 중 47%는 발작 증상이 멈춘다.
문제는 뇌전증 치료제 투여 환자 중 추가적으로 발작이 멈추는 환자 비율이 2차 치료에서는 13%, 3차 치료에서는 1~3%로 현저히 감소하다는 점이다.
이 때문에 환자 반응률을 높이기 위해 여러 약물을 병용투여하지만, 그럼에도 불응성 환자는 30~40%의 비율을 보인다. 불응성 환자를 타깃으로 한 약물이 필요한 이유다.
엑스코프리는 불응성 환자를 타깃으로 한다는 데 차별성을 갖는다.
실제 이전 1~3개 뇌전증 치료제를 복용하고 불응하는 부분발작 증상을 보이는 성인환자(18~70세)에게 엑스코프리를 투여하는 Study 013 임상과 Study 017 임상이 그 근거다.
임상 2a상인 Study 013 임상은 뇌전증 환자 221명을 대상으로 200mg의 엑스코프리 혹은 플라시보 약물을 6주간 적정 기간에 이어 6주간의 약물유지 기간을 두고 투여했다.
그 결과 발작 빈도가 줄어든 비율은 엑스코프리군이 55.6%, 플라시보군이 21.5%를 나타냈다.
발작 증세가 없어진 환자 비율은 엑스코프리군이 28.3%, 플라시보군은 8.8%였다.
임상 2b상인 Study 017 임상에서는 434명의 환자가 100mg(108명), 200mg(109명), 400mg(111명)의 엑스코프리 혹은 플라시보 약물을 18주간 투여받았다.
그 결과 엑스코프리 100mg, 200mg, 400mg를 투여한 환자 각각 35.5%, 55.0%, 55.0%에서 발작빈도가 줄었다.
발작 증세가 없어진 환자 비율은 100mg에서 4%, 200mg에서 11%, 400mg에서 21%로, 용량이 커질수록 높아졌다.
특히 두 임상에서 약물치료 유지기간 동안 통계적으로 유의미한 수의 환자들이 완전발작소실을 보였다.
뇌전증 치료 분야에서 최종 목표는 발작이 없어지는 효과인 만큼, 환자의 삶의 질에 직접적인 영향을 끼치고 있어 완전발작소실은 중요한 지표로 꼽힌다.
실제 엑스코프리는 Study013 사후분석 결과, 28%의 환자가 유지기간 동안 완전발작소실을 보였다. 반면 위약군은 9%에서 완전발작소실이 나타났다.
Study017 사후분석에서는 유지기간 동안 100mg, 200mg, 400mg 복용군에서 각각 4%, 11%, 21%가 완전발작소실을 달성했다.
SK바이오팜 박정신 임상개발실장은 "엑스코프리는 임상시험을 통해 통계적으로 유의미한 수의 환자들에게서 완전발작소실을 확인했다"며 "이는 환자 삶의 질 향상에 크게 기여할 수 있을 것"이라고 강조했다.
국내 출시 예고한 엑스코프리, UCB와 경쟁 구도
학계 "기존 약보다 좋은 건 알겠는데..."
이런 가운데 SK바이오팜이 엑스코프리의 국내 출시도 염두에 두고 있어 국내 뇌전증 치료제 시장도 치열해질 전망이다.
SK바이오팜 관계자는 "구체적 타임라인은 정해지지 않았지만, 엑스코프리의 국내 출시도 계획하고 있다"고 말했다.
현재 국내 뇌전증 치료제 시장은 절반 이상을 UCB가 이끌고 있다.
시장조사기관 유비스트에 따르면 UCB 케프라(성분명 레비티라세탐)는 2017년 250억원, 2018년 253억원의 처방액을 올린 데 이어 올해 3분기까지 184억원의 처방실적을 보였다.
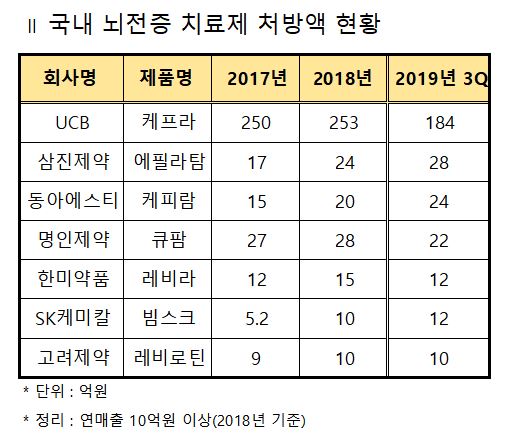
반면 100억원대 처방액을 보이는 국내 제약사의 제품은 없다.
삼진제약 에필라탐(성분명 레비티라세탐)이 올해 3분기 28억원의 누적 처방액을 올리며 가장 좋은 실적을 기록했고, 동아에스티 케피람(성분명 레비티라세탐) 24억원, 명인제약 큐팜(성분명 레비티라세탐) 22억원, 한미약품 레비라(성분명 레비티라세탐)와 SK케미칼 빔스크(성분명 라코사미드)가 각각 12억원을 기록하고 있다.
이런 시장 상황에서 미국 시장을 먼저 공략한 국내 신약이 국내 출시를 앞두고 있지만, 학계 반응은 미지근하다.
임상연구에 따르면 기존 치료제보다 '조금 더' 효과가 좋은 정도라는 것이다.
SK바이오팜에 따르면 Study 017 결과를 Bial 제비닉스(성분명 에스리카바제핀) UCB 브리비액트(성분명 브리바라세탐), 빔팻(성분명 라코사미드), 에자이 파이콤파(성분명 페람파넬) 등 다른 뇌전증 치료제와 비교했다.
그 결과 12주 유지요법 시점에서 약물에 반응한 환자 비율(50% 이상 발작 감소)은 기존 치료제는 40% 초반 수준이었고, 엑스코프리는 고용량 투여군에서 최대 64%로 나타났다.
한 대학병원 신경과 교수는 "임상연구 결과, 엑스코프리는 기존 치료제 대비 반응율이 많이 높은 정도는 아니었다"며 "기존 치료제들 보다 조금 더 효과가 있다는 데 의미가 있는 정도로, 획기적인 치료제라고 말하기 어렵다"고 말했다.
