당뇨병 약물의 근거구축 패러다임은 ‘안전한 혈당강하’에서 ‘심혈관 안전성 입증’으로 전환되어가는 경향을 보이고 있다. SGLT-2 억제제, DPP-4 억제제는 관련 심혈관 아웃컴 임상에서 심혈관 안전성 또는 혜택을 입증했다. 이런 가운데 최근 주요 심혈관 아웃컴 임상들의 신장기능 하위분석들이 다수 발표됐다.
만성 신장질환 등 신장기능장애는 당뇨병의 주요 합병증으로 꼽힌다. 혈당관리가 되지 않을 경우 당뇨병성 신장병증 발생 위험도가 높아지고 흡연, 비만, 고혈압, 이상지질혈증 등 동맥경화 위험인자가 동반됐을 경우 그 위험도는 더 높은 것으로 알려져 있다. 주요한 위험인자는 당뇨병과 고혈압으로, 잘 조절·관리되지 않고 유병기간이 길수록 신장질환 위험은 더 높은 것으로 보고됐다.
즉 신장기능은 조기관리의 유용성과 심혈관 관련 인자의 통합적 관리 효과가 전제된 상황에서 확인할 수 있는 안전성 평가지표로 볼 수 있다.
EMPA-REG OUTCOME 하위분석

심혈관 아웃컴 개선효과 입증으로 화두가 됐던 SGLT-2 억제제 엠파글리플로진은 EMPA-REG OUTCOME 하위분석(NEJM 2016;375:323-334)을 통해 신장질환 진행억제에 대한 효과를 입증한 바 있다.
이 분석에서는 EMPA-REG OUTCOME 연구에 참가한 환자들 중 사구체여과율(eGFR)이 30mL/min/㎡ 이상인 환자들을 엠파글리플로진 10 또는 25mg군, 위약군으로 분류해 거대단백뇨 진행, 혈청크레아티닌 수치 2배 이상 증가여부, 신장대체치료 시행, 신장질환으로 인한 사망, 단백뇨 발생 등을 평가했다.
그 결과 엠파글리플로진군에서는 12.17%, 위약군에서는 18.8%에서 신장병증이 악화돼 엠파글리플로진군의 위험도가 39% 낮았다(HR 0.61, 95% CI 0.53-0.70, P<0.001).
세부적으로 혈청 크레아티닌 2배 이상 증가한 환자 비율은 엠파글리플로진군 1.5%, 위약군 2.6%로 엠파글리플로진군의 위험이 44% 낮았고, 신장대체치료를 받은 환자는 각각 0.3%, 0.6%로 격차를 보였다. 단백뇨 발생률에서는 유의한 차이가 없었고 신장기능장애 프로파일도 유사한 경향을 보였다.
또 EASD 2016 포스터세션에서는 이 하위분석 연구를 연령에 따라 재분석한 결과도 발표됐다(poster number 1006). 이 분석에서는 우선 연령에 따라 만성 신장질환 위험도도 증가한다는 점을 전제하며 환자들을 65세 미만군, 65~75세 미만군, 75세 이상군으로 분류했다. 대상 환자들은 7020명으로 42개국에서 모집했고 평균 치료기간은 2.6년, 평균 관찰기간은 3.1년이었다. 베이스라인 A1C는 8% 전후였다. 베이스라인 eGFR은 65세 미만군은 80mL/min/1.73㎡ 전후, 65~75세 미만군은 68mL/min/1.73㎡, 75세 이상군은 62mL/min/1.73㎡였다. 안지오텐신전환효소(ACE) 억제제나 안지오텐신수용체차단제(ARB) 복용률은 80% 수준이었다.
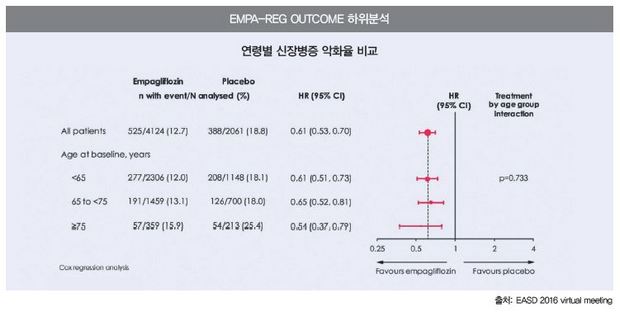
결과적으로 엠파글리플로진을 통한 신장병증 진행 예방효과는 전 연령대에서 고르게 나타났다. 65세 미만군에서는 39%(HR 0.61, 95% CI 0.51-0.73), 65~75세 미만군에서는 35%(0.65, 0.52-0.81), 75세 이상군에서는 46%(0.54, 0.37-0.79) 위험이 감소했다.
연구팀은 “EMPA-REG OUTCOME 분석결과 전반적인 신장관련 사건 발생률은 고령에서 높았고 이는 거대 단백뇨로 이어졌다”고 설명하는 한편 “기존 치료전략에 엠파글리플로진 추가투여를 통해 신장병증의 발생 또는 악화를 예방할 수 있었고 이는 모든 연령대에서 확인됐다”고 정리했다<그림>.
SAVOR-TIMI 53 하위분석
DPP-4 억제제인 삭사글립틴과 시타글립틴도 심혈관 아웃컴 임상인 SAVOR-TIMI 53, TECOS 하위연구를 통해 신장기능 관련 혜택을 입증했다. SAVOR-TIMI 53 하위분석 연구(Diabetes Care 10월 17일자 온라인판)에서는 삭사글립틴의 당뇨병성 신장병증 예방효과를 평가했다. 제2형 당뇨병 환자 1만 6492명을 삭사글립틴군과 위약군으로 무작위 분류해 평균 2.1년간 추적관찰했다.
베이스라인에서 58.8%(9696명)가 정상 단백뇨 수치(알부민/크레아티닌비<30mg/g)였고, 26.8%(4426명)는 미세단백뇨(ACR 30~300mg/g), 9.9%(1638명)가 거대단백뇨(ACR >300mg/g)였다.
분석결과 삭사글립틴 치료전략은 모든 단백뇨 카테고리에서 ACR 개선 혹은 악화 예방효과를 보였다. 2년 시점 삭사글립틴군과 위약군 간 평균 ACR 변화 차이는 사구체여과율(eGFR) >50mL/min/체표면적(BSA)에서 -19.3mg/g(P=0.033)이었고 eGFR 30~50mL/min/BSA에서는 -105mg/g(P=0.011), eGFR <30mL/min/BSA에서는 -245mg/g으로 나타났다. eGFR 감소에 따라 차이가 커졌다. 이는 1년, 2년, 연구종료 시점까지 일관된 경향을 보였고 ACR은 A1C와 연관성이 없었다.
한편 eGFR의 변화는 삭사글립틴군과 위약군에서 유사했다. 혈청 크레아티는 2배 증가, 만성 투석 시작, 신장이식, 혈청 크레아티닌 >6mg/dL 등 신장 안전성 관련 아웃컴도 유사하게 나타났다.
연구 주요저자인 이스라엘 하다쉬의대 Ofri Mosenzon 교수는 “삭사글립틴 치료는 ACR을 개선시켰고 정상 단백뇨에서도 일관된 효과가 나타났다”고 강조했고 “eGFR에 영향은 없었고, 혈당 조절에도 영향은 없었다”고 부연했다.
TECOS 하위분석

시타글립틴 역시 TECOS 연구 하위분석(Diabetes Care 10월 14일자 온라인판)을 통해 만성 신장질환에 대한 중립적인 입장을 확인했다. 이 분석에서는 TECOS 연구 참가자들 중 시타글립팁 투여군을 사구체여과율(eGFR) 기반으로 분류해 만성 심장질환 및 심혈관 아웃컴을 평가했다.
TECOS 연구는 1만 4671명을 이중맹검으로 시타글립틴군과 위약군으로 분류해 진행됐는데 이번 분석에서는 eGFR(mL/min/1.73㎡)에 따라 1(≥90), 2(60-89), 3a(45-59), 3b(30-44)에 따라 추가적으로 나눴다. 대상 환자들은 기존 치료전략은 지속적으로 투여받았다. 심혈관 및 만성 신장질환 아웃컴은 평균 3년 간 관찰했다.
분석결과 eGFR 3b에 해당하는 환자군은 더 고령이었고 여성이 많았으며 당뇨병 유병기간이 길었다. 주요 심혈관사건(4point MACE)은 eGFR이 낮을수록 높았다. eGFR 1단계에서는 3.52%, 2단계에서는 3.55%, 3a단계에서는 5.74%, 3b단계에서는 7.34%로 나타났다. eGFR 1단계를 기준으로 2, 3a, 3b단계의 위험정도를 비교했을 때 관련 인자들을 보정한 위험비(hazard ratio)는 각각 0.93(95% CI 0.82-1.06), 1.28(1.10-1.49), 1.39(1.13-1.72)였다. 모든 단계의 eGFR에서 시타글립틴은 심혈관 아웃컴과 연관성이 없었다.
신장기능은 모든 치료군에서 비슷한 감소율을 보였지만, 시타글립틴군에서 eGFR이 1.3mL/min/1.73㎡ 더 낮았다. eGFR에 대한 치료전략 간 차이는 환자거주 지역, 베이스라인 eGFR, 베이스라인 A1C, 평가시간 등을 보정했을 때도 유지됐다. 연구에서는 “신장기능장애는 심혈관 아웃컴 악화와 연관성을 보였고, 시타글립틴 자체는 심혈관 및 만성 신장질환 아웃컴에 임상적 영향을 미치지 않았다”고 정리했다.
시타글립틴 안전성 재확인
DPP-4 억제제와 신장기능 간 연관성은 이전 발표된 무작위 임상시험(Diabetes Care 9월 1일자 온라인판)을 통해서도 확인된 바 있다. 과체중 제2형 당뇨병 환자에서 DPP-4 억제제 시타글립틴이나 GLP-1 수용체 작용제 리라글루타이드의 신장 혈액역동학, 세관(tubular) 기능에 대한 영향을 평가한 연구로 베이스라인에서 CKD를 동반하지 않은 이들을 대상으로 했다.
무작위 이중맹검으로 인슐린을 투여받지 않은 제2형 당뇨병 환자 55명을 시타글립틴 100mg/day, 리라글루타이드 1.8mg/day, 위약으로 분류해 12주간 치료했다. 대상 환자들은 평균 연령 63세, BMI 31.8kg/㎡, 사구체여과율(GFR) 83mL/min/1.73㎡였다. 평균 알부민-크레아티닌비율(ACR)은 1.09mg/mmol이었다.
1차 종료점은 GFR 변화, 효과적인 신장 혈장유량(renal plasma flow)으로 설정했고 인슐린, 파라아미오마뇨산 청소율로 평가했다. 이와 함께 신장내 혈액역동학 변동성, 염분, 칼륨, 요소의 절대·분절배출량과 신장손상 마커(ACR, NGAL, KIM-1), 혈장 레닌 수치(PRC), 당화혈색소(A1C)도 함께 평가했다.
12주 시점 GFR을 평가한 결과 시타글립틴군은 위약군 대비 6mL/min/1.73㎡ 감소했고(P=0.17) 리라글루타이드군은 3mL/min/1.73㎡ 증가했다. 또 시타글립틴은 전반적으로 사구체압력을 감소시켰다.
ERPF, 다른 신장내 혈액역동학 변동성, 신장손상 마커, PRC는 양 치료군에서 변화가 없었고, A1C는 양군에서 감소했다. 단 2주 시점에서 시타글립틴은 나트륨, 요소 배출량 증가와 연관성을 보였다(P=0.005).
12주 평가한 결과 시타글립틴과 리라글루타이드는 신장 혈액역동학에 영향을 미치지 않았다 또 신장세관 기능 변화나 신장손상 마커의 변화도 관찰되지 않았다. 시타글립틴 유발성 사구체압력 감소의 타당성과 임상적 연관성은 여전히 고려해야할 부분으로 나타났다.
LEADER 하위분석

GLP-1 수용체 작용제인 리라글루타이드도 EASD 2016 구연발표 세션에서 발표된 LEADER 연구 하위분석을 통해 당뇨병성 신장질환 위험도 감소효과를 입증했다.
LEADER 연구는 심혈관질환이 있는 50세 이상 또는 다수의 심혈관질환 위험인자가 있는 제2형 당뇨병 환자 9340명을 리라글루타이드 0.6~1.8mg군과 위약군으로 구분해 3.5~5년간 추적관찰했다. 그 결과 54개월 시점에 심혈관 사망, 비치명적 심근경색증, 비치명적 뇌졸중을 포함한 3point-주요심혈관 유해사건 위험도는 리라글루타이드 군에서 13% 감소한 것으로 나타난 바 있다.
이번 분석에서는 당뇨병성 신장질환 진행위험을 분석했고 그 결과 리라글루타이드군에서 22% 위험이 감소했다(HR 0.78, 95% CI 0.67-0.92, P=0.003). 새로 발생한 지속성 거대 단백뇨, 혈청 크레아티닌 수치 2배 이상 증가, 지속적 신장대체치료 등 세부 위험도 모두 리라글루타이드군에서 낮았다. 단 신장질환으로 인한 사망위험은 높았다.
또 최근 발표된 이중맹검 임상시험(Diabetes Care 2016;39:206-213)에서도 일관된 결과가 확인된 바 있다. 이 임상시험에서는 투석에 의존하고 있는 말기신장질환 동반 제2형 당뇨병 환자에서 리라글루타이드를 통한 안전성과 효과 관련 파라미터를 평가했다.
말기 신장질환 동반 제2형 당뇨병 환자군(24명)과 정상 신장기능을 보이는 제2형 당뇨병 환자군(23명)을 비교했다. 환자군들은 리라글루타이드군과 위약군으로 분류됐고 리라글루타이드는 최대 1.8mg까지 증량했다.
최종 만성 신장질환 동반군 20명과 비동반군 20명을 비교한 결과 혈장 리라글루타이드 수치가 비동반군 대비 동반군에서 49% 높았다. 단 리라글루타이드로 인한 오심과 구토는 말기 신장질환 동반군에서 더 높았다.
전반적인 혈당관리율은 리라글루타이드군에서 더 개선됐고 또 베이스라인 인슐린 용량도 감소됐다. 체중은 리라글루타이드 투여 환자 중 말기 신장질환 동반군에서 -2.4kg, 비동반군에서 -2.9kg이었다.

