미국 NIH 추천 햄스터 효력시험에서 신속한 항바이러스+폐 염증억제 효과 입증
감염 후 3·5·7일차 RT-PCR 결과에서 항바이러스 효능 확인…연내 임상 착수
[메디칼업저버 정윤식 기자] 대웅제약이 코로나19(COVID-19) 치료제로 개발 중인 'DWRX2003(성분명 니클로사마이드)'의 식품의약품안전처 임상2상 IND(임상시험계획) 신청을 완료했다고 3일 밝혔다.
아울러 햄스터 효력시험에서 신속한 항바이러스 및 항염증 효과를 입증했다는 점도 강조했다.
대웅제약은 미국NIH(미국국립보건원)와의 DWRX2003 미팅에서 햄스터 모델에서의 효력시험을 요청받아 주식회사 노터스를 통해 해당 시험을 진행했다.
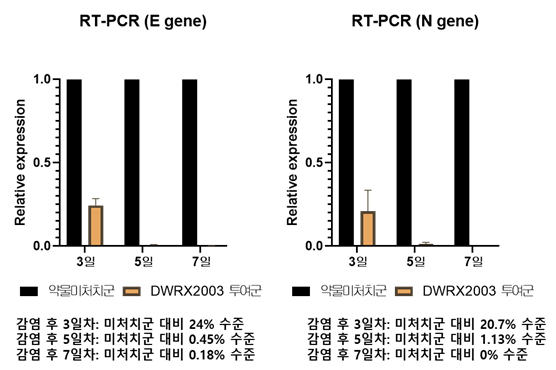
대웅제약의 설명에 따르면 감염 후 3·5·7일차에 확인된 RT-PCR 결과(바이러스 유전자 증폭검사), 감염이 극대화되는 3일차부터 강력한 항바이러스 효과를 나타냈고 특히, 5일차부터는 폐조직에서 상대적으로 바이러스 유전자가 거의 발현되지 않았다(단회투여).
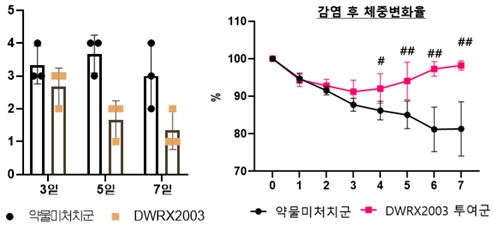
조직병리 시험결과에서도 병변이 현저히 개선됨을 확인했으며, 바이러스 감염 및 병세악화에 따라 나타나는 햄스터의 체중 감소 경향 또한 크게 완화됨을 확인했다.
이에 대웅제약은 지난 2일 식약처에 임상2상 IND를 신청하기에 이른 것.
대웅제약은 앞서 식약처와 질병관리청 산하 감염병연구소 등과의 협업을 통해 호이스타정의 임상2상 대상자 모집 및 투약을 신속하게 완료한 경험을 살려 DWRX2003의 임상2상 또한 최단기간 내에 완료한다는 계획이다.
DWRX2003의 임상2상 시험은 경증 및 중등증의 코로나19 환자 200명을 대상으로 연내 임상 착수를 준비 중이며, 해외 임상 1상에서의 안전성 자료를 바탕으로 미국 2상 IND 신청을 준비하고 있다.
대웅제약 전승호 사장은 "확진 즉시 투여를 통해 바이러스 제거와 동시에 증상을 신속히 개선시켜 입원기간을 단축시키고 의료환경을 정상화할 수 있는 강력한 코로나 치료제를 반드시 개발해내겠다"고 강조했다.
이어 "DWRX2003은 냉장 혹은 냉동 시설이 전혀 필요치 않으므로 국내유통 및 해외수출 시 큰 강점을 갖고 있어 제품의 공급 및 보관 관련 애로사항들을 최소화할 수 있을 것"이라고 덧붙였다.
대웅제약 박현진 개발본부장은 "초기 코로나 바이러스의 폐내 증식 및 폐손상을 억제하는 효과가 확인됐고 바이러스 감염 후 초기 폐손상을 억제하는 효과가 탁월한 것으로 보인다"며 "코로나 바이러스가 유도하는 급성 폐손상에 효과적인 대응책이 될 것으로 생각된다"고 말했다.

