[ISN 2019] SONAR 임상3상 결과, 콩팥병 동반 당뇨 환자 말기 신질한 진행 위험 35% ↓
2017년 아트라센탄 임상 중단…네덜란드 연구팀 "치료제 개발 계속 진행해야"

[메디칼업저버 박선혜 기자] 만성 콩팥병 동반 제2형 당뇨병 치료 신약 자리를 넘봤지만 고배를 마셨던 '아트라센탄(atrasentan)'이 다시금 주목받고 있다.
2017년 11월 중단됐던 SONAR 임상3상 데이터를 분석한 결과 아트라센탄이 만성 콩팥병 동반 제2형 당뇨병 환자의 신장 예후를 개선한 것으로 확인된 덕분이다.
당시 개발사는 예상보다 1차 종료점에 도달한 환자가 적어 SONAR 연구를 중단한다고 밝혔다. 이와 함께 치료제의 안전성 문제 때문에 연구를 중단하는 것은 아니라고 선을 그었다.
그러나 네덜란드 그로닝겐대학 의료센터 Dick de Zeeuw 교수팀이 제약사와의 제한된 협의 하에 SONAR 데이터를 분석한 결과, 아트라센탄의 치료 혜택이 확인됐다.
이에 따라 다른 회사에서 아트라센탄 개발을 이어가거나 아트라센탄의 문제점을 보완할 수 있는 치료제와의 병용요법을 고려해야 한다는 전문가 의견이 이어진다.
연구 결과는 14일 호주 멜버른에서 열린 세계신장학회총회(ISN 2019)에서 발표됐고 동시에 Lancet 온라인판에 실렸다.
장기간 치료에 따른 말기 신질환 진행 위험 평가
아트라센탄은 선택적 엔도텔린 A 수용체 길항제로, 제2형 당뇨병 환자는 단기간 아트라센탄 치료 시 유의미한 나트륨 저류(sodium retention) 없이 알부민뇨 감소 효과를 얻을 수 있다고 보고된다.
이번 연구는 장기간 아트라센탄 치료가 주요 신장 예후에 미치는 영향을 평가하고자 진행됐다.
이중맹검 무작위 위약 대조군 연구로 디자인된 임상3상에는 2013년 5월 17일부터 2017년 7월 13일까지 41개국 689곳에서 18~85세 제2형 당뇨병 환자 1만 1087명이 모집됐다. 여기에는 국내 환자 234명이 포함됐다.
전체 환자군의 추정 사구체여과율(eGFR)은 25~75mL/min/1.73㎡, 알부민-크레아티닌 비(UACR)는 300~5000mg/g였다. 이들은 최소 4주간 레닌-안지오텐신 시스템 억제제 최대 제품 용량 또는 최대 내약 용량을 복용하고 있었다.
약물 반응을 평가하기 위해 전체 환자군은 무작위 배정 전 매일 아트라센탄 0.75mg을 복용하는 농축 기간(enrichment period)을 가졌다.
이 기간에 체액 저류(fluid retention) 없이 UACR이 최소 30% 감소한 환자 총 2648명이 최종 이중맹검 연구에 포함됐다. 이들은 매일 아트라센탄 0.75mg 복용군(아트라센탄군, 1325명)과 위약군(1323명)에 무작위 분류됐다.
1차 종료점으로 혈청 크레아티닌 수치가 2배 증가해 30일 이상 지속되거나 말기 신질환으로 진행된 경우를 종합적으로 평가했다. 말기 신질환으로 진행은 △eGFR이15mL/min/1.73㎡ 미만으로 감소해 90일 이상 지속 △90일 이상 투석 시행 △신장이식 △신부전으로 인한 사망 등으로 정의했다.
신장 예후 개선 효과 얻었지만…체액 저류·빈혈 등 발생률 높아
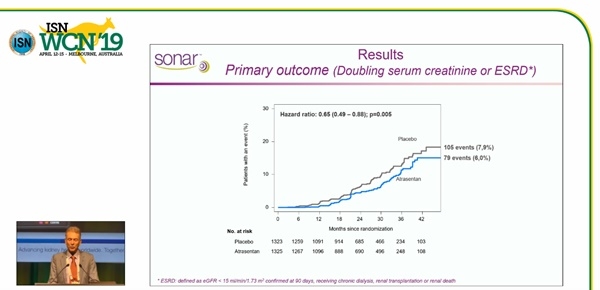
2.2년(중앙값)간 추적관찰한 결과, 1차 종료점 발생률은 아트라센탄군 6%(79명), 위약군 7.9%(105명)로 아트라센탄군의 1차 종료점 발생 위험이 35% 낮은 것으로 조사됐다(HR 0.65; 95% CI 0.49~0.88; P=0.0047).
아트라센탄으로 신장 예후 개선 혜택을 얻을 수 있었으나 안전성 측면에서는 문제가 감지됐다.
먼저 엔도텔린 A 수용체 길항제로 인한 체액 저류 및 빈혈은 아트라센탄군이 위약군보다 빈번하게 보고됐다. 혈량과다 또는 체액 저류 발생률은 아트라센탄군이 36.6%, 위약군이 32.3%로 아트라센탄군에서 약 4%p 더 높았고(P=0.022), 빈혈 발생률은 각각 18.5%와 10.3%였다(P<0.001).
체액 저류로 인해 나타날 수 있는 심부전 발생률도 아트라센탄군에서 더 높았다. 심부전으로 인한 입원율은 아트라센탄군 3.5%(47명), 위약군 2.6%(34명)로 약 1%p 차이가 벌어졌다. 단 심부전으로 인한 입원 위험은 아트라센탄군에서 1.33배 높았지만 통계적인 유의성은 없었다(HR 1.33; 95% CI 0.85~2.07; P=0.208).
아울러 사망률은 아트라센탄군 4.4%(58명), 위약군 3.9%(52명)로 두 군간 의미 있는 차이는 없었다(HR 1.09; 95% CI 0.75~1.59; P=0.65).
다만 아트라센탄군에서 안전성 문제가 나타났지만, 저용량을 복용하면 위험 대비 혜택의 균형을 맞출 수 있다는 게 연구팀의 전언이다.
"SGLT-2 억제제 병용으로 이상반응 문제 해결 가능할 것"
이번 결과에 따라 연구팀은 앞으로 아트라센탄 개발이 계속 진행돼야 한다고 강조했다.
Zeeuw 교수는 "이번 분석에서 아트라센탄 치료 효과가 명백하게 나타났다"며 "SONAR 연구는 중단됐지만, 이번 결과를 근거로 다른 회사에서 아트란센탄을 개발하거나 이러한 계열 치료제 개발에 관심을 가져야 할 것"이라고 피력했다.
이와 함께 아트라센탄을 카나글리플로진 등 SGLT-2 억제제와 병용하면 환자들이 얻는 혜택이 커질 것이란 전망도 나온다.
연구에 참여하지 않은 호주 모나쉬의대 Mark Cooper 교수는 "앞서 카나글리플로진 임상3상인 CREDENCE 연구에서 긍정적인 결과가 나왔다. SGLT-2 억제제는 이뇨작용이 있기에 아트라센탄과 병용한다면 아트라센탄의 체액 저류 등 주요 이상반응 문제를 해결할 수 있을 것"이라고 기대했다.

