
연세의대 교수
연세대세브란스병원 내과
최근 '간경화 치료에서 BCAA의 역할'을 주제로 2017 Liver Forum by Samil 심포지엄이 개최됐다. 연세의대 한광협 교수가 좌장을 맡은 가운데 Stanford University의 Prof. W Ray Kim, Kurume University의 Prof. Takumi Kawaguchi, 순천향의대 김상균 교수, 한양의대 전대원 교수가 차례로 강연하고 질의응답이 이어졌다. 본지에서는 이날의 강연 및 질의응답 내용을 요약·정리했다.
간성뇌증 관리의 최신지견

Stanford University
USA
간성뇌증의 정의
간성뇌증(hepatic encephalopathy, HE)의 발생 원인은 아직 정확히 알려지지 않았으며 진단할 수 있는 단일 증상 또는 징후도 없다. 간성뇌증은 간부전 또는 간문맥 차단에 의해 뇌기능 장애가 나타나는 질환으로, 임상 증상이 나타나지 않는 단계부터 혼수상태에 이를 수 있는 넓은 스펙트럼의 신경정신적 이상을 의미한다.
간성뇌증은 간경화의 치명적인 합병증으로, 3~4단계의 간성뇌증 환자는 1~2단계 간성뇌증 환자 대비 약 10배의 사망위험을 보인다. 다변량분석을 통해 다른 요인을 보정한 경우 3~4단계의 간성뇌증은 약 2.5배의 사망위험도를 나타냈다(HR 2.456, 95% CI 1.567-3.85, p<0.0001).
간성뇌증의 병인과 증상
간성뇌증 발생에는 혈중 암모니아 수치의 증가, GABA A 수용체의 변화, 성상세포(astrocyte)의 말초 benzodiazepine 수용체 증가, 신경스테로이드 생산 등 여러 요인이 복합적으로 작용하는 것으로 이해되고 있지만, 정확한 병인은 밝혀지지 않았다. 간성뇌증은 주의력, 시각-운동조화(visuo-motor coordination), 전신운동 속도(psychomotor speed), 작업기억(working memory), 반응억제(response inhibition) 등에 영향을 미치지만, 언어 능력, 지연기억, 언어적 또는 비언어적 지능에는 영향이 없다.
간성뇌증의 분류와 관리
간성뇌증은 급성 혹은 만성간질환에서 발생하는 폭넓은 신경정신학적 이상을 통틀어 일컫는다. 간성뇌증은 인지기능의 악화 정도에 따라 최소간성뇌증(minimal Hepatic Encephalopathy)과 1단계를 비현성간성뇌증(Covert HE) 그리고 2~4단계를 현성간성뇌증(Overt HE)이라 한다. 단계가 올라갈수록 인지기능이 악화하는데, 정상~1단계까지는 그 분류 기준이 모호하고 검사자 간 편차도 심하다. 하지만 2~4단계는 증상이 확연히 나타나므로 임상적 진단이 비교적 용이하다(hepatology. 2009;50:2014-21).
간성뇌증의 관리는 악화요인인 출혈, 고암모니아혈증, 전해질 불균형, 진정제 투여, 감염 및 변비 등을 우선 해결하고 간성뇌증 특이 치료를 시작하는 것, 재발 예방을 위한 유지요법으로 나눌 수 있다(Mayo Clin Proc. 2014;89:241-53)<그림 1>.
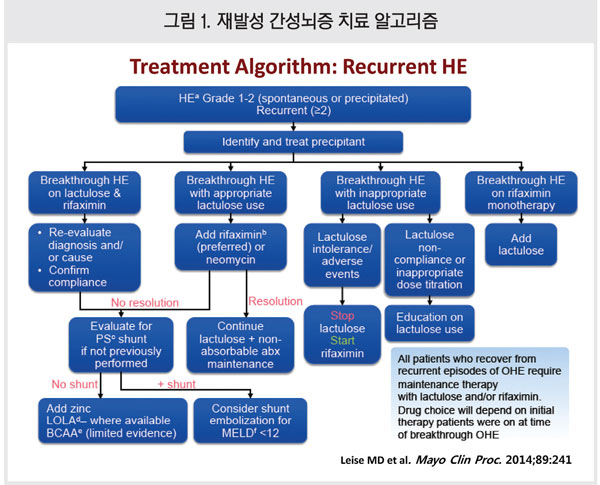
간성뇌증 환자의 영양 관리
기존에 많이 사용했던 단백질 제한식의 경우 간성뇌증의 중증도를 완화하는 데 별 도움을 주지 않는 것으로 밝혀졌으며(J hepatology. 2004;41:38-43) 환자의 이상적 체중을 기준으로 1일 35~40 kcal/kg을 섭취하고 단백질은 1일 1.2~1.5 g/kg 섭취가 권고된다. 식사 또는 보조적 유동식을 하루 전체에 걸쳐 균등히 배분해 섭취하고 늦은 저녁 시간에 간식을 섭취하도록 한다.
경구 식이를 통한 단백질 섭취가 불가능한 환자에서는 분지쇄아미노산(branched chain amino acid, BCAA) 보충제를 이용하면 질소섭취량을 권장량까지 섭취하는 데 도움이 된다(hepatology. 2014;60:715-35).
간성뇌증 치료 관련 임상시험
인도에서 진행된 임상연구에서는 간성뇌증이 나타난 환자를 대상으로 튜브를 이용해 간성뇌증 회복 전까지 최대 10일간 lactulose에 rifaximin 또는 위약을 추가 투여하는 것의 임상적 효과를 비교했다. 그 결과 rifaximin 추가 투여군은 단독 투여군 대비 간성뇌증으로부터의 회복률이 높았으며(76% vs 44%, p=0.004), 사망률 역시 추가 투여군이 단독 투여군 대비 월등히 낮은 결과를 보였다(24% vs 49%, p<0.05)(Am J Gastroenterol. 2013;108:1458-63).
Lactulose 섭취가 간성뇌증 재발을 어느 정도 방지하는지 알아본 임상시험에서는 치료군에서 위약군 대비 약 50% 낮은 재발률을 보였다(Gastroenterology. 2009;137:885-91). 분지쇄아미노산(branched-chain amino acid, BCAA) 섭취가 간성뇌증 발생에 미치는 영향을 분석한 16개의 논문을 메타분석한 결과 BCAA 섭취는 간성뇌증 재발을 27% 감소시키는 것으로 나타났다(Cochrane Database Syst Rev. 2003;2:CD001939). 또한 메타분석 결과, BCCA를 섭취하면 최소간성뇌증 발생 역시 30% 감소시켜 동일한 결과가 도출된 바 있다(Gluud. Cochrane Database of Systematic Reviews 2015, Issue 9. Art. No.: CD001939).
요약
간경화의 합병증인 간성뇌증은 사망률을 증가시키고 그에 대한 효과적인 예방치료가 존재한다. 현성, 일회성 간성뇌증은 악화요인을 찾아 치료하고 2차 발생의 예방이 필요하다. 치료는 lactulose, rifaximin, BCAA, 프로바이오틱 제제 등이 있다.
BCAA 효과: Beyond the Albumin

Kawaguchi
Kurume University
Japan
BCAA의 정의와 효용성
BCAA는 가지 형태의 구조를 가진 아미노산으로 valine, leucine, isoleucine을 의미한다. 일본에서는 2003년 저알부민증의 치료제로 승인받았으며, 이후 다른 질병에서도 효과가 보고됐다. 2005년에는 간부전을 개선한다는 것이 밝혀졌고 2006년에는 간암발생을 억제한다는 보고가 있었으며 2014년에는 환자의 생존율을 개선하는 것이 입증됐다.
BCAA의 간암 예방 효과
일본의 89개 기관에서 시행된 장기간의 무작위 배정 위약 대조 임상시험에서는 2년 이상의 추적관찰을 통해 BCAA 투여의 임상적 효과를 평가했다. 1차 평가 지표는 사망 또는 생명을 위협하는 사건(위식도 정맥류의 파열, 간부전, 간암)의 발생 건수로 설정했다.
그 결과 관찰기간에 식이조절을 한 대조군의 30%가 사망 또는 생명을 위협하는 사건을 1회 이상 경험했고 BCAA 투여군에서는 그 비율이 20%였다. BCAA 치료군은 전 원인 사망 및 정맥류 파열에서 대조군 대비 유의한 차이를 보이지 않았으나, 간부전 발생의 경우 50% 낮은 결과를 보였다(p=0.04). 전체 환자에서의 간세포암 발생률은 두 군 간 유의한 차이가 없었지만, BMI 25 이상의 비만 환자에서의 간암 발생률은 치료군이 2%, 대조군이 5%로 나타나 상당한 차이를 나타냈다(Clin Gastroenterol Hepatol. 2005;3:705-13).
BCAA의 간암 발생 위험을 BMI에 따라 계층분석한 추가 연구에서는 BCAA 치료가 BMI 25 이상의 간경화 환자의 간암 3년 발생률을 30% 감소시키는 것으로 나타났다(Hepatol Res. 2006;35:204-14). 하지만 BMI 가 25 미만인 환자 군에서는 이러한 차이가 발견되지 않았다. 따라서 BCAA의 간암 예방 효과에서 비만이 중요한 요인인 것이 밝혀졌다.
BCAA의 간암 억제 기전
BCAA는 phosphoinositide 3-kinase 수를 상향조절해 세포의 포도당 섭취를 상승시키고 혈당 수치를 내려 고인슐린혈증을 개선한다. 이로 인해 인슐린유사성장인자(Insulin-like growth factor, IGF)와 IGF-1 수용체의 활성을 감소시켜 세포 분화와 증식을 감소시키는 것으로 알려졌다(Hepatology. 2011;54:1063-70). 최근에는 BCAA가 간암 줄기세포 분화를 억제한다는 연구 결과도 발표됐다(PLoS One. 2013;8:e82346).
BCAA와 생존율 향상
낮은 BCAA 수치는 간경화 환자에서 부정적인 예후 인자로 알려졌다. 267명의 간암이 발생하지 않은 간경화 환자를 대상으로 진행한 임상연구에서는 BCAA 치료가 간부전과 감염의 위험을 줄여주어 간경화 환자의 생존율을 향상시키는 것으로 나타났다(Clin Gastroenterol Hepatol. 2014;12:1012-8)<그림 2>.
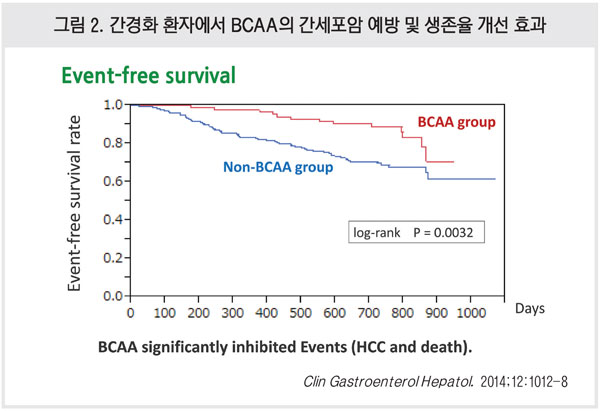
근감소증(sarcopenia) 역시 간경화 환자의 예후를 악화하는 요인으로 근감소증이 나타난 환자의 경우 근감소증이 나타나지 않은 환자 대비 5년 생존율이 약 20% 감소했다(Nutrition. 2015;31:193-9). 이 연구에서는 근감소증과 관련된 요인들을 data-mining 분석을 통해 조사했는데 BCAA 보충제를 투여한 환자군은 0.5 kg (중간값)의 근육 감소를 보인 반면, BCAA 비투여 환자군은 1.1 kg이 감소했다. 따라서 BCAA의 생존율 향상 효과는 근감소증을 예방하는 것과도 관련 있을 것으로 보인다.
진행된 간경화 환자에서 BCAA 투여의 효과

순천향의대 교수
순천향대학교병원
소화기내과
증례
HBsAg 양성인 56세 남성 환자로 복부 팽만과 간 이식 상담을 위해 내원했다.
여러 검사 결과 albumin 2.4 g/dL, bilirubin 3.2 mg/dL, PT (INR) 1.49, creatinine 1.1 mg/dL, HBeAg/Ab (-)/(+), HBV DNA negative, HCV Ab (-), HIV Ab (-), Child-Pugh class 10 C, MELD-Na 17점으로 나타났으며 항바이러스치료 경험은 없었던 점을 미루어 보아 과거에는 어땠는지 모르겠지만 현재 B형 간염이 임상증상에 영향을 미치지는 않는 것으로 판단했다.
이런 상황에서는 즉각적인 간 이식, 사망자 간 이식 대기, 경내경정맥 간내문맥 정맥단락술(transjugular intrahepatic portosystemic shunt, TIPS)를 통한 증상 완화, 약물치료와 식이조절 옵션이 있다. 이 환자는 생존 기증자가 없었던 관계로 사망 기증자를 기다리고 있었다. 현재 국내에서는 간이식 대기자 중 10%만이 기증을 받게 되며 이식을 못 받은 환자의 3개월 생존율은 75%로 조사된다(J Korean Soc Transplant. 2014;28:59-68).
이 환자는 대기자 등록 후 2년간 BCAA와 이뇨제를 투여하면서 관리 중인데 복수의 양이 점차 감소해 Child-Pugh class A와 MELD-Na 6점의 검사 결과를 보이는 등 매우 호전된 상태이다.
간경화 환자에서 BCAA 결핍 기전
과거에는 BCAA가 하나의 영양공급 수단으로 여겨졌다. 하지만 현재는 질병 자체의 진행을 변화시킬 수 있는 치료제의 역할을 한다는 근거들이 축적되고 있다. 특히, 만성 간질환과 진행된 간경화 환자에서는 체내 BCAA 수치가 저하되는 반면, 방향성 아미노산(aromatic amino acid) 수치는 증가한다. 이런 혈중 아미노산 구성의 변화가 유사(false) 신경전달물질을 만들어내고 간성뇌증의 발생을 유도한다는 이론이 제기됐으며 이러한 환자에서 아미노산의 공급이 치료에 중요한 역할을 할 수 있다.
간경화 환자에서 BCAA 감소 기전은 정확히 밝혀지지 않았지만 가장 유력하게 제기된 가설은 간내에서 urea cycle 부전에 의한 암모니아 대사 정체, 장 내 암모니아 흡수의 증가 등 고암모니아혈증이 가장 중요한 요인으로 지목된다.
우리 체내에서는 glutamate와 glutamine이 정교하게 균형을 이루고 있다. 암모니아 농도가 높아지면 glutamate를 기질로 한 glutamine의 생성이 촉진되는데, α-ketoglutarate가 glutamate로 전환될 때 BCAA가 필요하다. 즉, 고암모니아혈증은 BCAA의 사용을 증가시킨다.
BCAA 투여에 대한 메타분석 결과
2015년 발표된 메타분석 결과를 살펴보면 사망률에서는 BCAA 투여군과 비투여군 사이에 차이를 보이지 않았으나 전체적인 간성뇌증 발병은 BCAA군이 유의하게 낮았다. 현성 간성뇌증에서는 29%의 증상 감소가 유의미했지만 최소간성뇌증에서는 효과가 미미했다. Lactulose 또는 neomycin 투여군을 대조군으로 한 임상연구를 제외하고 분석했을 때는 BCAA의 효과가 두드러지는 것으로 나타났다. 이런 이유로 진료지침에서는 BCAA를 2차 치료제로 권고하고 있다.
BCAA 치료 관련 임상시험
2005년 일본에서 상당히 잘 고안된 대규모 임상시험 연구가 발표됐다. 600명 이상의 환자를 대상으로 2년간 BCAA 치료의 효과를 알아본 장기간 연구로 BCAA (12 g/day, n=314) 또는 식이조절(n=308)을 진행한 환자군을 비교했다. 1차 평가지표로는 간부전 악화, 위식도정맥류의 파열, 간암으로의 진행, 전 원인 사망률로 설정했다.
그 결과, BCAA 투여군의 무사건 생존율이 유의하게 높은 것으로 나타났다(HR 0.67, p=0.015). 또한, 치료기간 내에 BCAA 투여군의 알부민 수치가 대조군 대비 유의하게 상승했으며(p=0.018), 이러한 효과는 치료 6개월 시점부터 현저하게 나타났다. 결론적으로 BCAA를 장기간 투여했을 때 무사건 생존율과 알부민 수치의 개선을 기대할 수 있음이 증명됐다(Clin Gastroenterol Hepatol. 2005;3:705-13)<그림 3>.
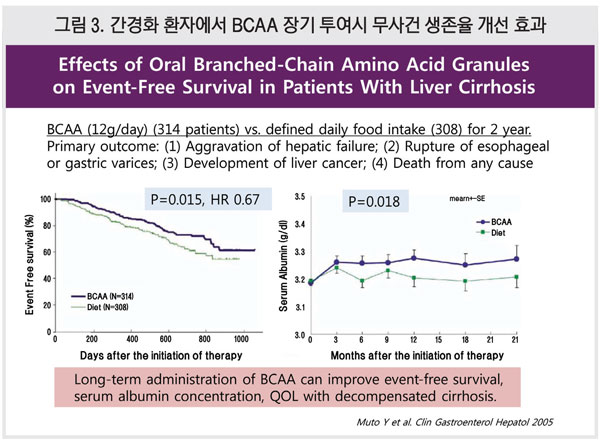
BCAA의 연구 동향
현재 간경화 환자를 대상으로 한 LIV-ACT 임상시험이 진행 중이다. 이 연구는 알부민 수치와 근육량에 미치는 BCAA의 영향을 알아본 첫 번째 연구로, 복수를 동반한 간경화 환자에서 BCAA의 6개월 투여가 혈청 알부민 수치를 상승시키는지와 BCAA를 1년 투여할 경우 근손실증이 개선되는지를 평가하기 위해 설계됐다. 추후 간성뇌증 예방에서 lactulose와 BCAA의 효과 비교, fibroscan 등을 통해 평가한 BCAA의 간섬유화 개선 효과 등의 연구가 필요할 것으로 생각한다.
최소간성뇌증의 진단과 치료

한양의대 교수
한양대서울병원
소화기내과
간성뇌증의 분류
간성뇌증은 간질환을 가진 환자에서 신경정신적 문제가 나타나는 것을 의미한다. 기존에는 간성뇌증 진단 후 생존 기간이 1년 정도 밖에 안 남은 경우가 많아 관심이 높지 않았다. 중증 간성뇌증의 경우 혼수상태가 나타나고 중등증일 경우 지남력 감소가 나타나는데, 최근 이러한 환자에 대한 관리가 잘 이뤄지면서 이보다 경증인 단계에도 관심이 늘고 있다.
경증으로 인해 약간의 불면증과 삶의 질 저하, 무기력증 등이 나타나는 것을 최소간성뇌증(minimal hepatic encephalopathy, MHE)이라 한다. 최근에는 의료기술이 발전하고 환자의 삶의 질 측면이 강조되면서 최소간성뇌증 관리의 중요성이 높아지고 있다.
최소간성뇌증의 증상
최소간성뇌증은 간경화 환자의 약 60%, 최소 40%에서 나타나는데 삶의 질을 상당히 저하시키며 신체 노동자의 업무 능력과 경제능력(투자 선택, 부동산 주식에서 부적절한 선택)을 현저히 저하시킨다. 현성 간성뇌증으로의 진행 위험이 높을 뿐더러 운전 능력을 저하시켜 교통사고의 위험을 증가시킨다(Am J Gastroenterol. 2007;102:1903-09.).
최소간성뇌증의 진단
최소간성뇌증의 진단은 연구자 또는 나라마다 기준이 다르다. 국제 간성뇌증 학회에서는 paper-pencil test 5종으로 조합한 간성뇌증 정신검사(psychometric hepatic encephalopathy score, PHES), 컴퓨터 기반 검사 및 신경생리(neurophysiological) 검사 중 적어도 두 가지를 다기관 임상시험의 평가지표로 사용하도록 권고한다.
간성뇌증 진단을 위한 컴퓨터 기반 검사로는 Critical Flicker Frequency test, Inhibitory Control Test, Stroop test가 권고된다. 현재 외국의 간성뇌증 관련 정신검사들의 경우 저작권이 있고 한국어판이 개발되지 않아 한국에서의 사용에 문제가 있다. 현재 11개 병원이 협력해 국내에서 사용할 수 있는 검사 도구를 만드는 작업이 진행 중이며 표준화 단계에 있다.
최소간성뇌증의 치료
현성 간성뇌증의 치료는 lactulose, rifaximin 주사제, rifaximin, L-ornithine-Lasparatate (LOLA) 주사제, 그리고 경구 BCAA를 치료제로 사용한다. 하지만 최소간성뇌증에 대해서는 구체적인 치료지침이 없는 상태이다. 현재 연구들은 체내 암모니아 수치를 감소시키는 방향으로 진행되고 있는데, 1) 생성을 억제하거나 2) 생성된 암모니아의 장 내 흡수를 막거나 3) 대사를 활성하거나 4) 방어력을 증진시키는 전략이 존재한다.
과거 체내 암모니아 발생원인 단백질의 섭취를 제한하는 치료가 행해졌는데, 환자의 영양부족과 근육량 감소시켜 생존기간이 단축되는 문제로 현재는 권고되지 않는다. 장 내 암모니아 생성 억제를 위해 항생제인 rifaximin을 사용해 장내세균을 사멸시키는 방법도 있다. 하지만 증상이 심하지 않은 최소간성뇌증 환자에서 항생제를 장기간 사용하는 것이 과연 안전한가에 대한 문제가 제기됐으며, 보험인정이 되지 않아 환자 부담이 크다.
Lactulose를 이용한 관장도 장내 암모니아를 효과적으로 제거하지만 관장을 지속적으로 하는 것이 어렵고 경구 투여시에는 잦은 설사로 인해 환자의 삶의 질이 매우 저하된다. 근육은 암모니아 대사가 가장 활발한 조직으로 BCAA 투여 시 근육량이 증가해 암모니아 수치를 저하시키고 근손실(sarcopenia)를 예방하는 효과가 있다(Nutr Clin Pract. 2013 Oct;28(5):580-8)<그림 4>.
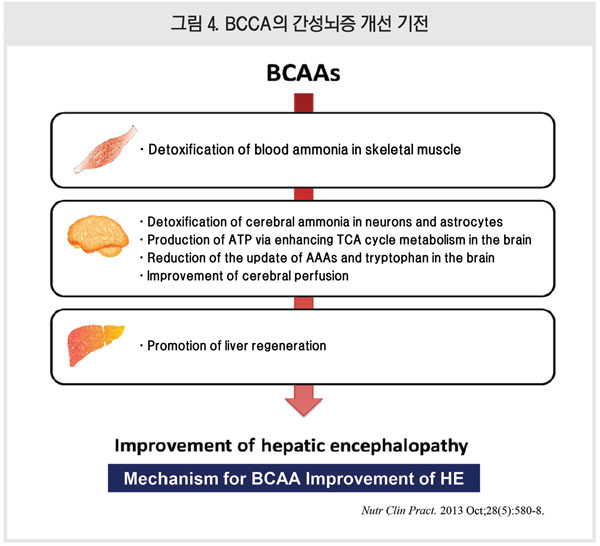
Q&A
Q: BCAA 치료가 간암 발생을 예방하는 효과가 있는지 임상시험에서 확인됐나요? 그리고 일본에서는 간암 예방을 위해 BCAA를 사용하고 있습니까?
A: 간암예방 효과는 임상적으로 증명됐지만 1차 평가항목은 아니었습니다. 대상자를 BMI에 따라 분류했을 때 비만 환자에서 간암 발생을 크게 억제하는 것으로 나타났습니다. 현재 BCAA는 간경화 환자 중 알부민 수치가 3.5 이하로 되어 있습니다만, 간암예방을 위해서도 간경병증 환자에게 처방이 가능합니다.
Q: 미국에서는 간성뇌증 환자에게 프로바이오틱 제제를 처방하는지 알고 싶습니다.
A: 미국에서 프로바이오틱 제제는 잘 사용하지 않습니다. 진료지침에서 권고되지도 않고 그제제의 구성을 정확히 알지 못하기 때문에 만성간질환 환자에게 투여하는 것이 위험하다고 생각합니다. 프로바이오틱 제제는 일반 상점에서도 살 수 있지만, 간성뇌증 임상시험에서 사용한 균주와 다른 종류일 가능성이 매우 높고, 품질 관리가 제대로 되고 있는지도 불명확하기 때문입니다.
정리·메디칼라이터부
사진·김민수 기자

